オーダーメイドの遺伝子治療が理論から実践へ
小児の希少疾患は、もはや単なる科学的な珍事として扱われていない。Nature Medicine に掲載された新たな書簡で、研究者グループは、それらが患者1人のために設計された治療を含む、カスタムメイドの細胞・遺伝子治療の候補としてますます注目されていると論じている。
著者らは、注目すべき最近の変化を指摘する。かつては事実上治療不可能だった遺伝性疾患で、今では1回投与の遺伝子治療が有意で持続的な利益をもたらしている。この変化自体も重要だが、論文は、より大きな混乱は構造的なものだと主張する。すなわち、規制当局、開発者、医療制度が、従来の医薬品開発の前提に当てはまらない医薬品に直面しているということだ。
この書簡によれば、1人の患者を対象とする試験はもはや仮説ではない。著者らは、超希少な神経疾患において、患者に合わせたアデノ随伴ウイルス遺伝子治療が開発され、3年以内に投与された例を挙げている。また、さらに迅速な例として、患者特異的なベース編集治療が作成され、規制当局の承認を経て、致死的な代謝疾患をもつ新生児に約8か月で投与されたケースも取り上げている。
これらの例は、個別化治療の科学面と製造面が急速に進歩していることを示している。著者らが言うように、より難しい問題は、こうした治療を少数の例外的なケースだけでなく、より多くの子どもたちが利用できるようにする道筋を築くことだ。
アクセスの問題は今や科学だけでなく経済の問題でもある
この書簡は、アクセスを中心的なボトルネックとして位置づけている。カスタム遺伝子治療が現実味を増している一方で、希少疾患の子どもの大半はいまだ有効な治療を受けられていない。この格差を、論文は科学の失敗だけとは捉えていない。むしろ、従来の医薬品の商業モデルは、高度に個別化された治療には適していないと主張する。
このミスマッチはすでに市場に表れている。著者らは、遺伝子治療の先駆けとなったバイオテクノロジー企業が商業的に持続するのに苦戦し、命を救う有効性があるにもかかわらず製品を撤退した例もあると指摘する。要するに、問題は治療が効くかどうかだけではない。極めて少数の患者、あるいは1人の子どもを対象とする製品を、資金調達、承認、製造、持続供給するために作られた制度が支えられるのか、という点にある。
それはこの分野の核心に矛盾を生む。治療がより精密に個別化されるほど、従来の営利型医薬品モデルが報いるような拡張可能な製品からは遠ざかる。一般的な疾患では、大規模試験と広い市場が何年にもわたる投資を正当化できる。しかし、超希少な小児疾患では、同じモデルが推進力ではなく障壁になりうる。
書簡は、制度が変わらなければ、個別化治療は信頼できる治療カテゴリーではなく、孤立したブレークスルーとして現れ続けるだろうと論じている。
開発と規制をつなぐための枠組み
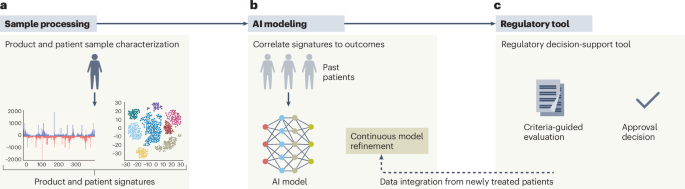
論文は、製品の特性評価から規制判断までをつなぐ道筋として、UNICORN フレームワークと呼ぶものを提示している。ここで示された書簡の抜粋には、このフレームワークの運用詳細はすべて書かれていないが、著者らの議論から目的は明確だ。すなわち、オーダーメイドの遺伝子治療を、大量市場向け医薬品のために設計された承認経路に無理やり当てはめることなく、反復可能な評価構造を作ることだ。
これは重要だ。なぜなら、標準的なモデルは大規模コホート、再現可能な製造ロット、広範な商業的検証に強く依存しているからだ。超希少な小児治療では、そうした特徴が何一つない場合がある。それでも規制当局は品質、安全性、見込まれる有益性を評価しなければならないが、治療が1人の子どもの変異、時間軸、臨床経過に合わせて設計される場合、必要とされるエビデンスの形は異なるかもしれない。
したがって、この書簡は、製品の特性評価と規制審査を結びつけ、厳密性を保ちながら個別化治療が本質的に異なる製品であることを認める、より適応的なモデルを示している。
その根底にあるメッセージは、基準を緩めるべきだということではない。むしろ、基準を新しい形式に翻訳する必要があるかもしれない、ということだ。治療が1人の患者のために作られるなら、承認の論理は数万人向け製品に使われるのと同じ前提に依拠することはできない。
なぜ小児希少疾患が圧力点なのか
この圧力が最も強く表れるのが小児希少疾患だ。患者数は少なく、進行は速く、遅れは生涯にわたる影響を及ぼしうる。著者らが挙げた2つの例は、その緊急性を際立たせている。オーダーメイド治療に3年の開発期間を要するのは、歴史的な医薬品開発基準から見てもすでに異例に圧縮されている。設計から規制承認、そして新生児への治療までが約8か月という道のりは、さらに劇的だ。
こうした時間軸は、この分野の可能性と脆弱性の両方を示している。科学、製造、規制、臨床ニーズが一致すれば、オーダーメイド治療は驚くべき速さで進められることを示している。同時に、難しい問いも突きつける。例外的なケースでこれが起きるなら、体系的に実現するには何が必要なのか、という問いだ。
書簡は、その答えは単なる研究室での革新の追加ではなく、より良い制度設計でもあると論じている。小児希少疾患には、しばしば代替治療も大きな商業市場もない。だからこそ、それらは、医療が規模ではなく必要性を中心に開発システムを構築できるかどうかを試す試金石となる。
この提案が分野に示すもの
この論文の意義は、1つの治療法を発表することよりも、旧来の制度が吸収しきれない速度で新しい薬剤カテゴリーが到来していると認めた点にある。著者らは、オーダーメイドの遺伝子治療が技術的に可能で、臨床的にも意味がある一方で、構造的には提供が難しい世界を描いている。
もし彼らの主張が正しければ、将来の小児希少疾患の進歩は、より良いベクターや編集ツール、製造法だけでなく、個別化治療を持続的な現実として認識する承認経路にも依存することになる。書簡は、希少疾患医療がすでにその段階に入ったと示している。
これは重要な変化だ。長年、パーソナライズされた遺伝子治療は最前線の野心として語られてきた。ここで挙げられた例は、それが今や科学的課題であると同時に、行政上・規制上の課題にもなっていることを示している。次のブレークスルーは、規制当局と開発者が単発の成功を実用的なシステムへと変えられるかどうかにかかっているかもしれない。
壊滅的な小児疾患に向き合う家族にとって、この違いは抽象的ではない。それによって、オーダーメイド医療が例外のままでいるのか、それとも旧来のモデルに収まりきらないほど希少な疾患の通常診療の一部になり始めるのかが決まる可能性がある。
この記事は Nature Medicine の報道に基づいています。元記事を読む。
Originally published on nature.com