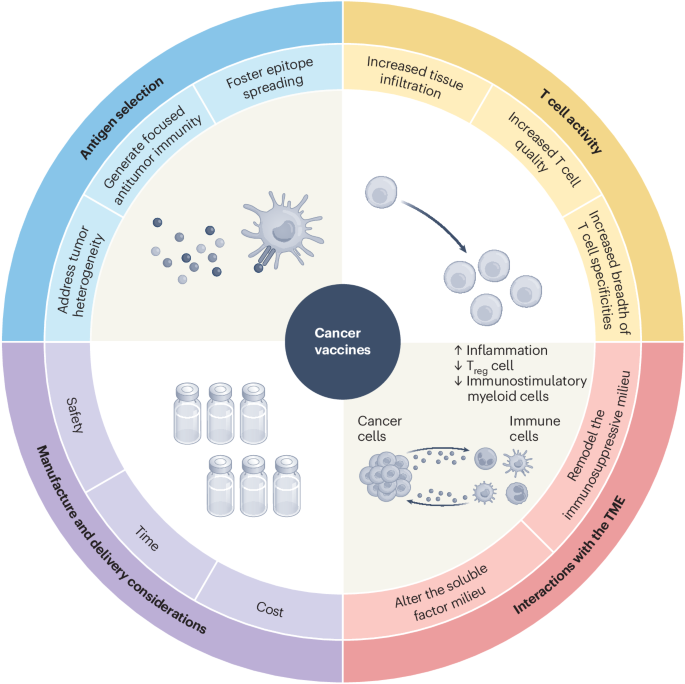
がん治療における新しいフロンティア
がんワクチンは医学の歴史において独特の地位を占めています。100年以上にわたって追求されてきた治療概念ですが、最近になって臨床的に有意な方法で機能させるために必要な生物学的理解と技術的ツールを習得しました。Nature Medicineに掲載された包括的なレビューは、現在の分野の状態を調べ、初期の挫折から現在臨床試験を通じて真の約束を持って進んでいる洗練されたmRNAと新抗原標的アプローチへの道をたどっています。
レビューのタイミングは、その分野における真の加速を反映しています。COVID-19ワクチンを搭載したmRNA技術プラットフォームは、驚くべき速度でがん応用に適応され、個人化されたがんワクチンプログラムからの初期臨床データは、多くの年間がんワクチン接種の商業的実行可能性に懐疑的だった製薬会社から数十億ドルの投資を引き付けるのに十分励ましいものでした。2026年の状況は、わずか5年前とは根本的に異なります。
がんワクチンは感染性疾患の伝統的なワクチンとは異なる原則で機能します。ワクチンが曝露前に病原体を認識するように免疫系を訓練するのではなく、がんワクチンは、既に体内に存在する腫瘍細胞を認識し、破壊するように免疫系を訓練することを目的としています。この治療ワクチン接種アプローチでは、腫瘍細胞上の分子標的を正確に特定する必要があります。そこで、腫瘍細胞を外物としてマークし、腫瘍が免疫クリアランスから身を守るために作成する免疫抑制環境を克服するのに十分強い免疫応答を生成します。
個人化されたmRNAがんワクチン
現在臨床開発中の科学的に最も先進的ながんワクチンアプローチは、mRNA技術を使用して、個々の患者の腫瘍に固有の変異タンパク質フラグメントである新抗原を標的とする個人化されたワクチンを作成します。これらの標的は各患者のがん細胞の特定の変異によって作成されるため、正常な組織には存在せず、免疫攻撃の高度に選別された標的となります。
個人化されたワクチン開発プロセスには、患者の腫瘍をシーケンスして特定の変異を識別する、計算ツールを使用して変異したペプチドが腫瘍細胞表面に表示され、免疫細胞によって認識される方法を予測する、これらの標的をコードするmRNAワクチンを合成する、免疫応答を刺激するためにワクチンを投与することが含まれます。腫瘍のシーケンスからワクチン投与までのパイプライン全体は、わずか数年前は数ヶ月かかっていた高度な製造環境で数週間かかります。
ModernaとMerkは、彼らのmRNA-4157候補でこの分野の臨床開発を主導してきました。これは、チェックポイント阻害剤pembrolizumabとの組み合わせで、ランダム化第2相試験でメラノーマ再発の統計的に有意な減少を示しました。これは、分野を電動化し、その後、複数のがん種への拡大につながった結果です。Nature Medicineレビューは、肺、結腸直腸、膀胱、および他のがん種を横切った個人化されたmRNAワクチンを評価している、より広い分野のコンテキストでこの結果を配置します。
共有抗原ワクチンと組み合わせアプローチ
すべてのがんワクチンプログラムが個人化されているわけではありません。共有抗原ワクチンは、多くの患者の腫瘍全体で過剰発現されるタンパク質を標的とします。HER2、MAGE、および腫瘍関連炭水化物抗原などの標的は、既製品開発をサポートするのに十分一般的で、潜在的により単純な製造とより低いコストがあります。これらのアプローチは、個人化された新抗原の特異性の一部と、スケーラブル製造と標準化された臨床開発の実用的な利点を交換します。
がんワクチンをチェックポイント阻害剤、CAR-T療法、または他の免疫療法モダリティと組み合わせるアプローチは、主要な調査領域として浮上しています。理由は、ワクチンが腫瘍特異的免疫応答を促進し、チェックポイント阻害剤がこれらの応答を抑制するために腫瘍が使用するブレーキを除去します。これにより、どちらのアプローチも単独で達成できない相乗的な抗腫瘍活動が生じる可能性があります。これらの組み合わせからの臨床データは、複数の腫瘍型全体で蓄積されています。
レビューは、ワクチン配信システムの高まる洗練さを強調しています。これには、腫瘍抗原提示用に最適化された脂質ナノ粒子、過度な毒性なしに免疫活性化を強化する新規アジュバント製剤、および現在のインビボプログラミング可能なアプローチが含まれます。これらは、エクスビボ製造ステップではなく、内因性細胞機構を使用して個人化された免疫応答を生成します。
課題と未解決の質問
真の進展にもかかわらず、がんワクチン分野は、Nature Medicineレビューが直接対処する重大な課題に直面しています。腫瘍免疫逃避 - がん細胞が抗原発現をダウンレギュレートし、免疫抑制マイクロ環境を作成し、免疫攻撃への耐性を発展させる能力 - は依然として基本的な障害です。強い初期免疫応答を生成するワクチンでも、腫瘍が刺激する免疫応答を回避するために進化した場合、持続的な腫瘍制御をもたらさない可能性があります。
患者の選択は不完全に理解されています。いくつかの腫瘍型といくつかの患者はがんワクチンアプローチに劇的に反応しているようですが、他の患者は最小限の利益を示し、応答の生物学的予測因子はまだ十分に特徴付けられておらず、治療決定を確信を持ってガイドすることはできません。ワクチン応答を予測するバイオマーカーを特定することは、分野全体において主要な研究優先事項です。
特に個人化されたワクチンでは、製造コストと複雑性は、広く使用できるようにするための障害のままです。患者の腫瘍をシーケンスし、標的を特定し、個別化されたワクチンを設計および合成し、臨床的に意味のあるタイムラインで投与するプロセスは、かなりのインフラストラクチャを含み、依然として高価です。プロセスイノベーションと製造スケールを通じてこれらのコストを削減することが、個人化されたがんワクチンが完全な患者人口の可能性に達するために必要になります。
前進
Nature Medicineレビューは、分野の軌道についての適度な楽観主義で締めくくられています。現在、複数の第3相試験は、第2相データが十分に説得力があり、投資を正当化するのに十分な設定でがんワクチン候補について進行中です。これらの大規模な試験からの結果は今後数年で到着し、がんワクチンが実験的から腫瘍学の実践における標準的な治療法にどのように迅速に移動するかを大幅に決定します。
mRNAプラットフォーム技術、AI駆動の新抗原予測、迅速な腫瘍シーケンス、および腫瘍免疫学の検証の融合は、以前の世代の研究者が達成できない方法でがんワクチン接種が成功するための可能な条件を作成しました。その分野が最終的に免疫システムを広く適用可能ながん治療に変える約束を果たすかどうかは、まだ不明ですが、臨床証拠は現在、その可能性を真剣に受け止めるのに十分な強度です。
この記事はNature Medicineのレポートに基づいています。元の記事を読む。