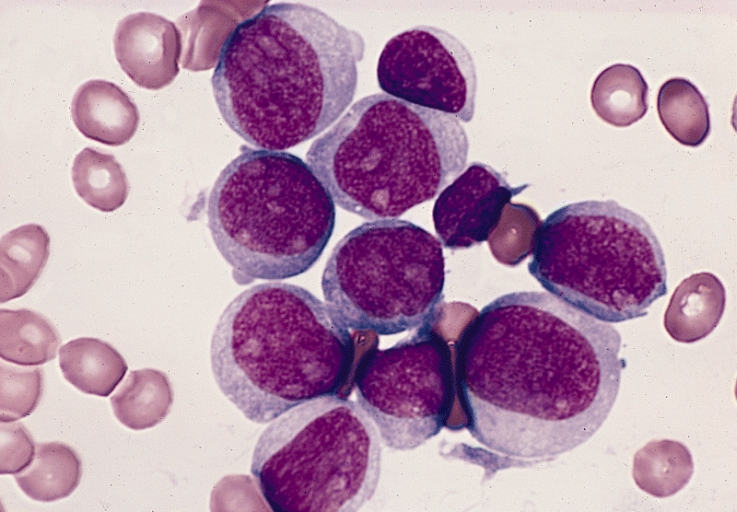
FDA अलीकडील नकाराचा पुन्हा आढावा घेत आहे
अमेरिकेची अन्न आणि औषध प्रशासन संस्था दुर्मिळ कर्करोगावरील उपचार Ebvallo वर पुन्हा विचार करत आहे, ज्याला काही महिन्यांपूर्वी अनपेक्षितपणे नाकारण्यात आले होते. दिलेल्या STAT candidate metadata आणि मूळ मजकुराच्या आधारे, मुख्य नवीन घडामोड अशी आहे की Ebvallo विकसित करणाऱ्या कंपन्यांनी FDA सोबत असा करार केला आहे ज्यामुळे एजन्सीने पूर्वी हा उपचार का नाकारला होता, त्या मुख्य कारणाचे निराकरण करता येईल.
हा बदल मर्यादित असला तरी महत्त्वाचा आहे. नकारानंतर पुन्हा समीक्षा सुरू होणे याचा अर्थ असा की तो वाद अंतिम नव्हता, आणि नियामकांनी ओळखलेल्या किमान एका मुख्य प्रश्नासाठी आता उपायाचा मार्ग उपलब्ध झाला असावा.
हे का महत्त्वाचे आहे
FDA चे निर्णय परत घेणे किंवा पुन्हा उघडणे याकडे बारकाईने पाहिले जाते, कारण यामुळे एकाच वेळी अनेक गोष्टी सूचित होऊ शकतात: नियामक दृष्टीकोनात बदल, प्रायोजकांकडून नवीन पुरावे किंवा बांधिलकी, किंवा अपेक्षेपेक्षा कमी अपूर्ण प्रश्न. या प्रकरणात उपलब्ध स्रोत सामग्री फक्त मर्यादित निष्कर्षालाच पाठिंबा देते: सुरुवातीच्या नकाराचे मुख्य कारण संबधित मुद्द्यावर डेव्हलपर्स आणि FDA यांनी करार केल्यानंतर एजन्सी आता त्या उपचाराचा पुन्हा विचार करत आहे.
दिलेल्या मजकुरात सार्वजनिक तपशील मर्यादित असले तरीही ते स्वतःमध्ये महत्त्वाचे आहे. दुर्मिळ-कर्करोग औषध विकास अनेकदा छोट्या लोकसमूहांमध्ये पुढे जातो, जिथे उपचार पर्याय कमी असतात आणि मोठ्या सामान्य-रोग कार्यक्रमांपेक्षा लाभ-जोखीम संदर्भ वेगळा असतो. रुग्ण, डॉक्टर आणि गुंतवणूकदारांसाठी, बंद फाइल आणि पुन्हा उघडलेल्या पुनरावलोकनातील फरक मोठा असू शकतो.