遺伝子編集移植アプローチが早期の臨床マイルストーンに到達
Nature Medicineに掲載されたヒト初の研究は、高リスク急性骨髄性白血病および骨髄異形成症候群の患者向けに設計された、CRISPR-Cas9で編集した同種造血細胞移植の初期臨床結果を報告している。この治療戦略では、CD33標的を除去したドナー細胞を用いることで、正常なドナー由来骨髄系細胞に同等のリスクを与えることなく、CD33標的薬ゲムツズマブ オゾガマイシンを移植後に使用できるようにしている。
このアプローチの理屈は単純だが、技術的には野心的である。高リスクAMLやMDSの患者は、同種造血細胞移植後であっても再発しうる。移植後維持療法の難点の一つは、残存白血病を抑制・排除するための治療が、健康なドナー細胞にも損傷を与えうることだ。この試験の治験製品であるtremtelectogene empogeditemcel、またはtrem-celは、輸注前にドナー移植片からCD33を除去することで、この問題の一部を解決しようとしている。
第1/2a相試験で何が分かったか
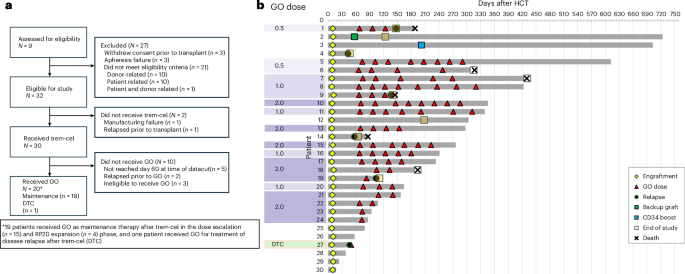
多施設共同の非盲検第1/2a相試験は、再発リスクが高いとみなされたAMLまたはMDSの成人患者を登録した。骨髄破壊的前処置の後、患者はtrem-celを投与された。その後、一部の参加者は28日周期で0.5 mg/m2から2.0 mg/m2の範囲でゲムツズマブ オゾガマイシンによる維持療法を受けた。
主要安全性評価項目は28日目までの好中球生着だった。公表報告によると、trem-celを受けた30人全員がこの評価項目を達成した。好中球生着までの中央値は10日で、95%信頼区間は9日から10日だった。生着遅延や不全はあらゆる移植戦略の中心的リスクであり、とくにゲノム編集されたドナー細胞を用いる戦略では重要であるため、この点は大きい。
19人が移植後のゲムツズマブ オゾガマイシン維持療法を受け、そのうち15人は第1相の用量漸増部分、4人は第2相の用量拡大部分に含まれていた。試験では、ゲムツズマブ オゾガマイシンは推奨第2相用量である2 mg/m2まで安全に忍容されたと報告されている。論文はまた、試験が早期に中止され、完了した第1相部分を含む最終報告であることも示している。