Terapias gênicas sob medida estão saindo da teoria e indo para a prática
As doenças pediátricas raras já não são tratadas apenas como curiosidades científicas. Em uma nova correspondência publicada na Nature Medicine, um grupo de pesquisadores argumenta que elas estão se tornando cada vez mais candidatas a terapias celulares e gênicas feitas sob medida, incluindo tratamentos concebidos para um único paciente.
Os autores apontam para uma mudança recente marcante. Distúrbios hereditários que antes eram praticamente intratáveis agora estão vendo terapias gênicas de dose única produzirem benefícios significativos e duradouros. Essa mudança já é importante por si só, mas o artigo argumenta que a disrupção maior é estrutural: reguladores, desenvolvedores e sistemas de saúde agora estão lidando com medicamentos que não se encaixam nas premissas do desenvolvimento farmacêutico convencional.
De acordo com a correspondência, ensaios com um único paciente já não são hipotéticos. Os autores citam uma doença neurológica ultrarrara na qual uma terapia gênica com vírus adeno-associado, personalizada, foi desenvolvida e administrada em três anos. Eles também destacam um caso ainda mais rápido, em que uma terapia de edição de base específica para um paciente foi criada, aprovada pelos reguladores e administrada a um recém-nascido com um distúrbio metabólico letal em cerca de oito meses.
Esses exemplos sugerem que o lado científico e de fabricação da terapia individualizada está avançando rapidamente. O problema mais difícil, argumentam os autores, é construir um caminho que torne esses tratamentos alcançáveis para mais crianças, e não apenas para um punhado de casos extraordinários.
O problema de acesso agora é tão econômico quanto científico
A correspondência enquadra o acesso como o principal gargalo. Mesmo com terapias gênicas personalizadas se tornando mais viáveis, a maioria das crianças com doenças raras ainda não tem acesso a tratamento eficaz. O artigo não descreve essa lacuna como uma falha apenas da ciência. Em vez disso, argumenta que o modelo comercial convencional dos medicamentos é pouco adequado a terapias altamente individualizadas.
Esse descompasso já é visível no mercado. Os autores observam que empresas de biotecnologia que ajudaram a inaugurar as terapias gênicas têm lutado para permanecer comercialmente viáveis e, em alguns casos, retiraram produtos apesar da eficácia que salva vidas. Em outras palavras, o problema não é apenas se uma terapia pode funcionar. É se as instituições criadas para financiar, aprovar, fabricar e sustentar tratamentos conseguem apoiar produtos voltados a populações extremamente pequenas de pacientes, ou até a uma única criança.
Isso cria uma contradição no centro do campo. Quanto mais precisamente uma terapia é ajustada, menos ela se parece com o tipo de produto escalável que o modelo tradicional de medicamento com fins lucrativos foi projetado para recompensar. Para doenças comuns, grandes ensaios e mercados amplos podem justificar anos de investimento. Para distúrbios pediátricos ultrarraros, esse mesmo modelo pode se tornar uma barreira em vez de um motor.
A correspondência argumenta que, se o sistema não mudar, as terapias individualizadas podem continuar surgindo como avanços isolados em vez de uma categoria de tratamento confiável.
Uma estrutura pensada para ligar desenvolvimento e regulação
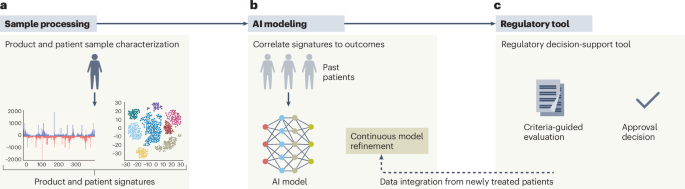
O artigo apresenta o que chama de estrutura UNICORN, proposta como um caminho da caracterização do produto à tomada de decisão regulatória. O trecho da correspondência fornecido aqui não detalha todos os aspectos operacionais dessa estrutura, mas sua finalidade é clara a partir do argumento dos autores: criar uma estrutura repetível para avaliar terapias gênicas sob medida sem forçá-las a se encaixar em vias de aprovação criadas para medicamentos de mercado de massa.
Isso importa porque o modelo padrão depende fortemente de grandes coortes, lotes de fabricação repetíveis e validação comercial extensa. Terapias pediátricas ultrarraras podem não ter nenhuma dessas características. Um regulador ainda precisa avaliar qualidade, segurança e provável benefício, mas o conjunto de evidências pode precisar parecer diferente quando o tratamento é desenhado em torno da mutação, do cronograma e da trajetória clínica de uma criança.
A correspondência, portanto, aponta para um modelo mais adaptável, capaz de conectar a caracterização do produto e a análise regulatória de modo a preservar o rigor sem ignorar que terapias individualizadas são produtos fundamentalmente diferentes.
A mensagem subjacente não é que os padrões devam ser enfraquecidos. É que talvez precisem ser traduzidos para um novo formato. Se uma terapia é feita para um paciente, a lógica de aprovação não pode se basear nas mesmas premissas usadas para um produto destinado a dezenas de milhares.
Por que a doença rara pediátrica é o ponto de pressão
A doença rara pediátrica é onde essa pressão se torna mais aguda. Os pacientes são poucos, a progressão pode ser rápida e os atrasos podem ter consequências por toda a vida. Os dois exemplos citados pelos autores reforçam essa urgência. Um prazo de desenvolvimento de três anos para uma terapia personalizada já é historicamente comprimido pelos padrões do desenvolvimento de medicamentos. Um caminho de oito meses entre o desenho, a liberação regulatória e o tratamento de um recém-nascido é ainda mais dramático.
Esses prazos mostram tanto a promessa quanto a fragilidade do campo. Eles demonstram que terapias sob medida podem avançar com rapidez notável quando ciência, fabricação, regulação e necessidade clínica se alinham. Eles também levantam uma pergunta difícil: se isso pode acontecer em casos excepcionais, o que seria necessário para que acontecesse de forma sistemática?
A correspondência argumenta que a resposta não é apenas mais inovação laboratorial. É também melhor desenho institucional. Doenças raras pediátricas muitas vezes não têm tratamento de reserva nem grande mercado comercial. Isso as torna um teste para saber se a medicina consegue construir sistemas de desenvolvimento em torno da necessidade, e não da escala.
O que esta proposta sinaliza para o campo
A importância do artigo está menos em anunciar uma única terapia do que em reconhecer que uma nova categoria de medicamento está chegando mais rápido do que os sistemas legados conseguem absorver. Os autores descrevem um mundo em que terapias gênicas sob medida estão se tornando tecnicamente possíveis, clinicamente significativas e, ainda assim, estruturalmente difíceis de entregar.
Se o argumento deles estiver correto, o progresso futuro em doenças pediátricas raras dependerá não apenas de vetores melhores, ferramentas de edição ou métodos de fabricação, mas também de vias de aprovação que reconheçam terapias individualizadas como uma realidade duradoura. A correspondência sustenta que a medicina de doenças raras já entrou nessa fase.
Essa é uma mudança importante. Durante anos, a terapia gênica personalizada muitas vezes soou como uma ambição de fronteira. Os exemplos citados aqui sugerem que ela está se tornando agora um desafio administrativo e regulatório tanto quanto científico. Os próximos avanços podem depender de os reguladores e desenvolvedores conseguirem transformar sucessos pontuais em um sistema viável.
Para famílias que enfrentam distúrbios infantis devastadores, essa distinção não é abstrata. Ela pode determinar se a medicina sob medida continuará sendo a exceção ou se passará a fazer parte do cuidado de rotina para doenças raras demais para se encaixar no modelo antigo.
Este artigo é baseado em reportagem da Nature Medicine. Leia o artigo original.
Originally published on nature.com