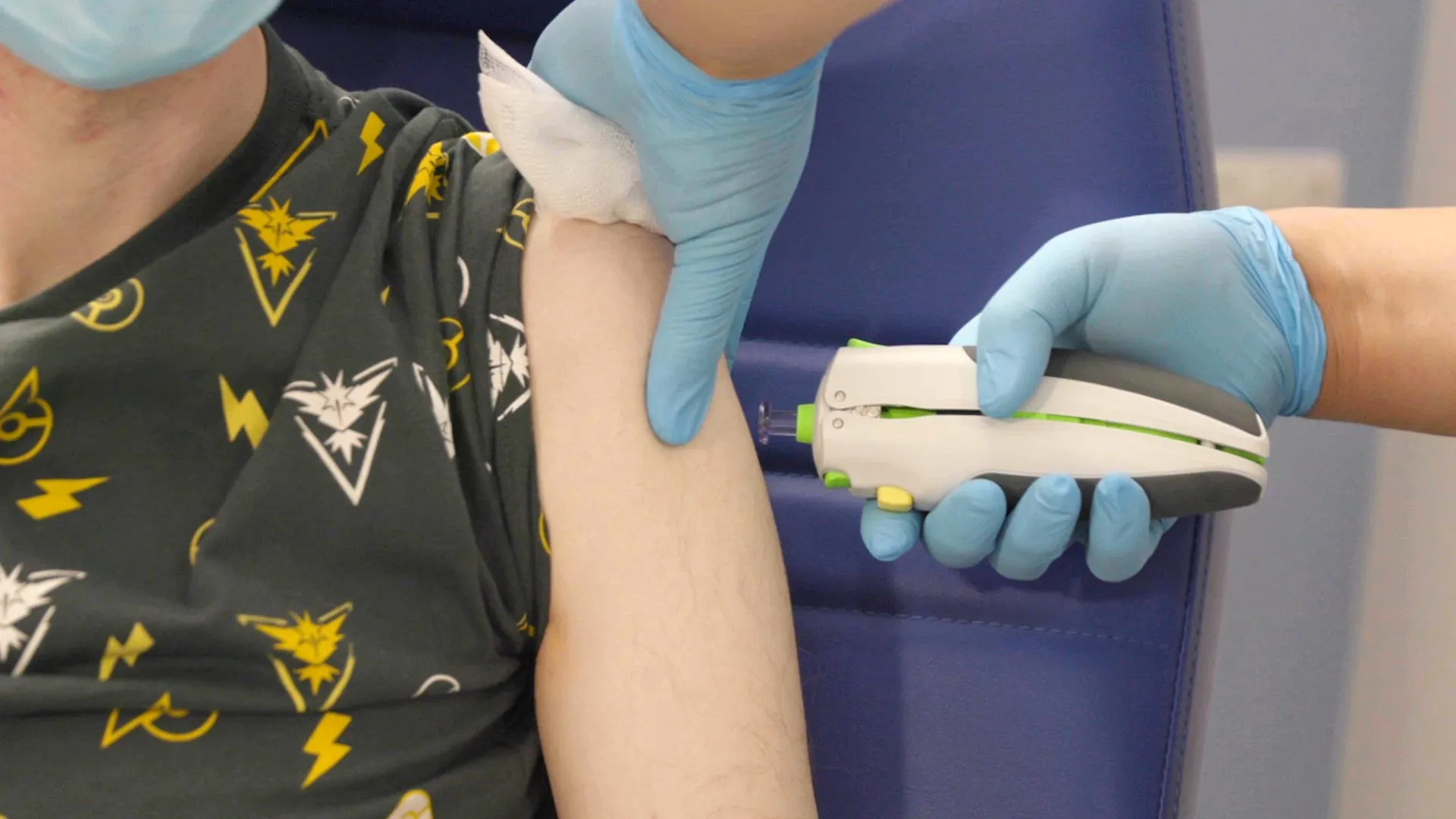
古い約束が再び臨床の場に戻ってきた
老化研究には、破られた約束が尽きない。理論上は画期的に見えても、実際には期待外れに終わった化合物や仕組みが、何度も持ち上げられてきた。その歴史が、今回の部分的リプログラミングへの関心の高まりを特に注目すべきものにしている。提示された New Scientist の記事によれば、加齢に伴う視覚障害を対象とする臨床試験が、生命科学における最も野心的な若返りの発想の一つを、再び真剣な検証の対象にしている。
この概念は、2006 年の山中伸弥と高橋和利による画期的発見にさかのぼる。彼らは、4 つの遺伝子を導入することで成熟細胞を人工多能性幹細胞へと巻き戻せることを示した。この発見は、専門化した成体細胞が最終的な身分に固定されているわけではないことを示し、再生医療を変えた。原理的には、より若く柔軟な状態へと再設定できるのだ。
なぜ完全なリプログラミングではだめだったのか
人工多能性幹細胞の治療上の魅力は明らかだった。損傷した組織を患者自身の体から得た新しい細胞で置き換えられるなら、多くの変性疾患は治療可能になるかもしれない。だが、この方法の強力さには問題が内在していた。細胞を完全にリセットすると、心筋細胞を心筋細胞たらしめる、あるいは網膜細胞を網膜細胞たらしめる、その同一性そのものが失われる。とりわけ体内で直接使う場合、これは重大な安全性と制御の課題を生む。
部分的リプログラミングは、そのリセットの若返り効果だけを取り出し、胚の状態まで完全に戻らないようにする試みだ。細胞老化の特徴の一部を巻き戻しつつ、細胞の中核機能を保つことを目指す。これが安定して実現できれば、損傷した組織は完全に一から作り直さなくても機能を取り戻せるかもしれない。
なぜ眼が理にかなった出発点なのか
New Scientist の記事が取り上げる加齢関連の視覚障害の臨床試験は、象徴的だ。眼科疾患は実験医学の先頭に立つことが多い。組織にアクセスしやすく、結果を精密に測定でき、しかも全身ではなく局所治療が可能な場合があるからだ。そのため眼科は、肝臓や脳のような臓器で最初に試しにくいアプローチを検証する実用的な試験場になる。
視力低下は、若返り生物学の核心的な約束とも一致する。加齢関連疾患の多くは、単一の急性損傷ではなく、細胞の徐々の衰えによって引き起こされる。もし部分的リプログラミングが老化した網膜細胞や関連細胞の機能を回復できれば、「若返り」が実験室のレトリックから臨床効果へ移れることを示す、これまでで最も明確な例の一つになるだろう。
それでも慎重さは必要だ
提示された記事は慎重であり、他の誰もがそうであるべきだ。老化研究は何度も過剰な期待の波にさらされてきた。レスベラトロール、カロリー制限模倣薬、MTOR を標的とする戦略、そして老化細胞除去薬は、大きな期待を生んだ。中には依然として科学的価値のあるものもあるが、かつて示唆されたような率直なアンチエイジング革命を実現したものはない。
部分的リプログラミングは、その歴史に強みとリスクの両方を伴って入ってくる。その科学的系譜は、現代細胞生物学の基礎的発見の一つから生まれているため、以前の多くの流行よりはるかに確かなものだ。同時に、細胞の同一性を操作することは本質的に高リスクだ。治療が細胞のリセットに近づくほど、安全性、持続性、制御の重要性は増す。
成功が本当に意味するもの
視力試験で良い結果が出たとしても、医学が全身の老化を「逆転」する方法を発見したことにはならない。だが、それよりも具体的で、おそらくより重要なことを意味する。つまり、細胞老化の中核的な仕組みが、患者のもとで制御された臨床環境の中で変えられるかもしれないということだ。それだけでも、投資を動かし、後続試験を加速させ、再生医療にこれまでの見出しを飾った多くの約束よりも明確な道筋を与えるには十分だ。
この話の本当の意義は、不老不死の話ではない。生物学的基盤を持ち、臨床的に検証可能な若返りへの道が、再び姿を現したことだ。長年の失望のあと、部分的リプログラミングは単純だが決定的な問いを突きつけられている。細胞は、まったく別のものにならずに若返ることができるのか。答えはスローガンではなく、今まさに注目を集め始めているような慎重な試験を通じて示される。
この記事は New Scientist の報道に基づいています。元記事を読む。
Originally published on newscientist.com