Las terapias génicas a medida pasan de la teoría a la práctica
Las enfermedades pediátricas raras ya no se consideran solo curiosidades científicas. En una nueva correspondencia publicada en Nature Medicine, un grupo de investigadores sostiene que cada vez más se están convirtiendo en candidatas para terapias celulares y génicas diseñadas a medida, incluidos tratamientos concebidos para un solo paciente.
Los autores señalan un cambio reciente llamativo. Trastornos hereditarios que antes eran, en la práctica, intratables ahora están viendo cómo las terapias génicas de una sola administración producen beneficios significativos y duraderos. Ese cambio ya es importante por sí mismo, pero el artículo sostiene que la disrupción mayor es estructural: los reguladores, los desarrolladores y los sistemas de salud están afrontando medicamentos que no encajan con los supuestos del desarrollo farmacéutico convencional.
Según la correspondencia, los ensayos con un solo paciente ya no son hipotéticos. Los autores citan una enfermedad neurológica ultrarrara en la que se desarrolló y administró en tres años una terapia génica con virus adenoasociado diseñada a medida. También destacan un caso aún más rápido en el que una terapia de edición de bases específica para un paciente fue creada, aprobada por los reguladores y administrada a un recién nacido con un trastorno metabólico letal en aproximadamente ocho meses.
Esos ejemplos sugieren que la parte científica y de fabricación de la terapia individualizada avanza con rapidez. El problema más difícil, argumentan los autores, es construir una vía que permita que estos tratamientos lleguen a más niños y no solo a un puñado de casos extraordinarios.
El problema de acceso es ahora tanto económico como científico
La correspondencia sitúa el acceso como el principal cuello de botella. Incluso a medida que las terapias génicas personalizadas se vuelven más viables, la mayoría de los niños con enfermedades raras sigue sin acceso a un tratamiento eficaz. El artículo no describe esa brecha como un fracaso únicamente científico. En cambio, sostiene que el modelo comercial convencional de los productos farmacéuticos se adapta mal a terapias altamente individualizadas.
Esa descoordinación ya es visible en el mercado. Los autores señalan que las empresas biotecnológicas que ayudaron a abrir camino en las terapias génicas han tenido dificultades para seguir siendo comercialmente viables y, en algunos casos, han retirado productos pese a su eficacia para salvar vidas. En otras palabras, el problema no es solo si una terapia puede funcionar. Es si las instituciones creadas para financiar, aprobar, fabricar y sostener tratamientos pueden respaldar productos dirigidos a poblaciones de pacientes extremadamente pequeñas, o incluso a un solo niño.
Eso crea una contradicción en el centro del campo. Cuanto más precisamente se adapta una terapia, menos se parece al tipo de producto escalable que el modelo farmacéutico tradicional con fines de lucro está diseñado para recompensar. Para las enfermedades comunes, los ensayos grandes y los mercados amplios pueden justificar años de inversión. Para los trastornos pediátricos ultrarraros, ese mismo modelo puede convertirse en una barrera en lugar de un motor.
La correspondencia sostiene que, si el sistema no cambia, las terapias individualizadas podrían seguir apareciendo como avances aislados en lugar de como una categoría de tratamiento fiable.
Un marco pensado para tender un puente entre desarrollo y regulación
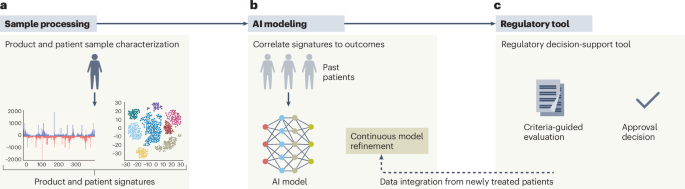
El artículo presenta lo que llama el marco UNICORN, planteado como una ruta desde la caracterización del producto hasta la toma de decisiones regulatorias. El extracto de la correspondencia que se ofrece aquí no detalla todos los aspectos operativos de ese marco, pero su propósito es claro en el argumento de los autores: crear una estructura repetible para evaluar terapias génicas a medida sin obligarlas a encajar en vías de aprobación diseñadas para medicamentos de mercado masivo.
Eso importa porque el modelo estándar depende en gran medida de grandes cohortes, rondas de fabricación repetibles y una validación comercial extensa. Las terapias pediátricas ultrarraras pueden no tener ninguna de esas características. Un regulador sigue teniendo que valorar la calidad, la seguridad y el beneficio probable, pero el paquete de evidencia puede necesitar ser diferente cuando el tratamiento se diseña alrededor de la mutación, el calendario y la trayectoria clínica de un solo niño.
Por ello, la correspondencia apunta hacia un modelo más adaptable, uno que pueda conectar la caracterización del producto y la revisión regulatoria de manera que preserve el rigor al tiempo que reconoce que las terapias individualizadas son productos fundamentalmente distintos.
El mensaje subyacente no es que deban debilitarse los estándares. Es que los estándares quizá deban traducirse a un nuevo formato. Si una terapia se fabrica para un paciente, la lógica de aprobación no puede basarse en los mismos supuestos utilizados para un producto destinado a decenas de miles.
Por qué la enfermedad rara pediátrica es el punto de presión
La enfermedad rara pediátrica es donde esta presión resulta más aguda. Los pacientes son pocos, la progresión puede ser rápida y los retrasos pueden tener consecuencias de por vida. Los dos ejemplos citados por los autores subrayan esa urgencia. Un plazo de desarrollo de tres años para una terapia a medida ya está históricamente comprimido según los estándares del desarrollo farmacéutico. Un recorrido de ocho meses desde el diseño hasta la autorización regulatoria y el tratamiento en un recién nacido es todavía más dramático.
Esos plazos muestran tanto la promesa como la fragilidad del campo. Demuestran que las terapias a medida pueden avanzar con una velocidad notable cuando la ciencia, la fabricación, la regulación y la necesidad clínica convergen. También plantean una pregunta difícil: si esto puede ocurrir en casos excepcionales, ¿qué haría falta para que ocurriera de forma sistemática?
La correspondencia sostiene que la respuesta no es solo más innovación de laboratorio. También es un mejor diseño institucional. Las enfermedades raras pediátricas a menudo no tienen tratamiento alternativo ni un gran mercado comercial. Eso las convierte en una prueba de si la medicina puede construir sistemas de desarrollo alrededor de la necesidad y no de la escala.
Qué señala esta propuesta para el campo
La importancia del artículo reside menos en anunciar una terapia concreta que en reconocer que una nueva categoría de medicina está llegando más rápido de lo que los sistemas heredados pueden absorberla. Los autores describen un mundo en el que las terapias génicas a medida se vuelven técnicamente posibles, clínicamente significativas y, aun así, estructuralmente difíciles de entregar.
Si su argumento se sostiene, el progreso futuro en las enfermedades pediátricas raras dependerá no solo de mejores vectores, herramientas de edición o métodos de fabricación, sino también de vías de aprobación que reconozcan las terapias individualizadas como una realidad duradera. La correspondencia sostiene que la medicina de las enfermedades raras ya ha entrado en esa fase.
Ese es un cambio importante. Durante años, la terapia génica personalizada a menudo sonaba como una ambición de frontera. Los ejemplos citados aquí sugieren que ahora está convirtiéndose tanto en un reto administrativo como regulatorio. Los próximos avances pueden depender de si los reguladores y los desarrolladores pueden transformar los éxitos puntuales en un sistema viable.
Para las familias que afrontan trastornos infantiles devastadores, esa distinción no es abstracta. Podría determinar si la medicina a medida sigue siendo la excepción o empieza a formar parte de la atención rutinaria para enfermedades demasiado raras como para encajar en el modelo antiguo.
Este artículo se basa en información de Nature Medicine. Leer el artículo original.
Originally published on nature.com