Una opción oral de seguimiento para un problema familiar de obesidad
Una de las partes más difíciles del tratamiento de la obesidad no es perder peso en primer lugar, sino conservar esas mejoras cuando la terapia cambia o se suspende. Un nuevo estudio de fase 3b en
Nature Medicine
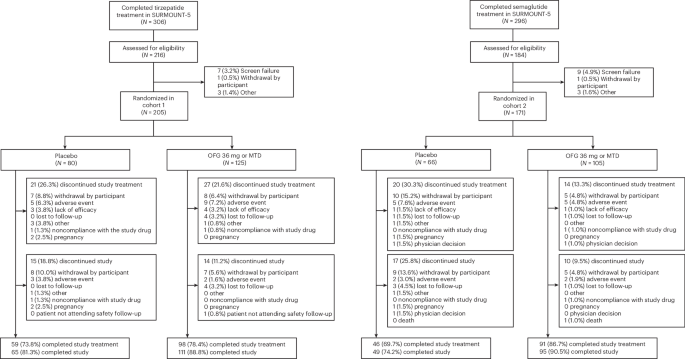
aborda directamente ese problema de mantenimiento, evaluando si un agonista oral del receptor GLP-1, administrado una vez al día, puede ayudar a las personas a conservar la pérdida de peso ya lograda con medicamentos inyectables.El fármaco es orforglipron, un agonista oral no peptídico del receptor GLP-1. En el ensayo ATTAIN-MAINTAIN, publicado recientemente, los investigadores reclutaron a personas que previamente habían sido tratadas con tirzepatida o semaglutida durante el estudio SURMOUNT-5. Luego, los participantes fueron aleatorizados, en un diseño doble ciego y controlado con placebo, para recibir orforglipron oral diario o placebo.
La pregunta central era práctica y clínicamente importante: después de que los pacientes alcanzaran una meseta de peso corporal con terapia inyectable, ¿podía un medicamento oral ayudarles a conservar más de esa reducción durante el año siguiente?
Qué encontró el ensayo
La respuesta, según este estudio, fue sí. Entre los participantes del cohorte con experiencia previa en tirzepatida que habían alcanzado una meseta de peso, quienes fueron asignados a orforglipron mantuvieron una estimación basada en modelos del 74,7% de su reducción de peso corporal en la semana 52. El grupo placebo mantuvo el 49,2%. Eso produjo una diferencia estimada de tratamiento de 25,5 puntos porcentuales, con un valor de P reportado por debajo de 0,001.
Los resultados también fueron sólidos en el cohorte con experiencia previa en semaglutida. Los participantes con orforglipron mantuvieron una estimación basada en modelos del 79,3% de su reducción de peso en la semana 52, en comparación con el 37,6% del placebo. La diferencia estimada de tratamiento fue de 41,7 puntos porcentuales, nuevamente con P < 0,001.
El artículo señala además que se cumplieron todos los criterios de valoración secundarios clave, aunque el resumen no detalla cada uno individualmente. También informa mejoras en factores de riesgo cardiometabólicos y un perfil de seguridad en general similar al de los agonistas inyectables del receptor GLP-1.
Los eventos adversos más comunes fueron gastrointestinales, descritos en su mayoría como de intensidad leve a moderada. Ese detalle importa porque la tolerabilidad suele determinar si una terapia puede funcionar fuera de entornos de ensayo estrictamente controlados.