Un enfoque de trasplante editado genéticamente alcanza un primer hito clínico
Un estudio de primera en humanos publicado en Nature Medicine informa resultados clínicos iniciales de un trasplante alogénico de células hematopoyéticas editado con CRISPR-Cas9, diseñado para pacientes con leucemia mieloide aguda de alto riesgo y síndrome mielodisplásico. La estrategia de tratamiento utiliza células del donante a las que se les ha eliminado el objetivo CD33, lo que permite a los médicos seguir el trasplante con el fármaco dirigido a CD33 gemtuzumab ozogamicina sin exponer a las células mieloides normales derivadas del donante al mismo nivel de riesgo.
La lógica detrás del enfoque es sencilla, pero técnicamente ambiciosa. Los pacientes con AML o SMD de alto riesgo pueden recaer incluso después del trasplante alogénico de células hematopoyéticas. Un reto en el mantenimiento posrasplante es que las terapias destinadas a suprimir o eliminar la leucemia residual también pueden dañar las células sanas del donante. El producto en investigación de este ensayo, tremtelectogene empogeditemcel, o trem-cel, pretende resolver parte de ese problema eliminando CD33 del injerto del donante antes de la infusión.
Lo que encontró el ensayo de fase 1/2a
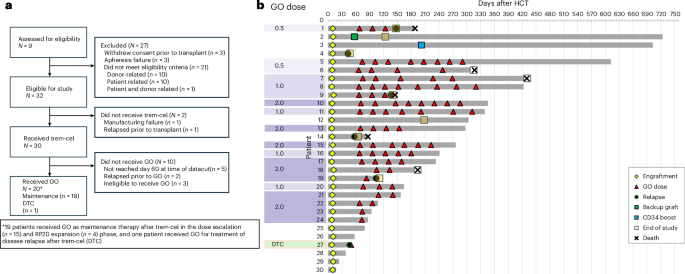
El estudio multicéntrico y abierto de fase 1/2a incluyó a pacientes adultos con AML o SMD considerados de alto riesgo de recaída. Tras un acondicionamiento mieloablativo, los pacientes recibieron trem-cel. Algunos participantes pasaron luego a recibir mantenimiento con gemtuzumab ozogamicina en ciclos de 28 días, con dosis de 0,5 mg/m2 a 2,0 mg/m2.
El criterio principal de seguridad fue el injerto de neutrófilos para el día 28. Según el informe publicado, los 30 pacientes que recibieron trem-cel cumplieron ese criterio. El tiempo mediano hasta el injerto de neutrófilos fue de 10 días, con un intervalo de confianza del 95% de 9 a 10 días. Esto importa porque el injerto retrasado o fallido es uno de los riesgos centrales de cualquier estrategia de trasplante, especialmente en una que implica células donantes editadas genéticamente.
Diecinueve pacientes recibieron mantenimiento posrasplante con gemtuzumab ozogamicina, incluidos 15 en la parte de escalada de dosis de fase 1 y cuatro en la expansión de dosis de fase 2. El estudio informa que gemtuzumab ozogamicina se toleró de forma segura hasta la dosis recomendada de fase 2 de 2 mg/m2. El artículo también señala que el ensayo se detuvo antes de tiempo y sirve como informe final, incluyendo la parte completada de fase 1.