Ein genetisch editierter Transplantationsansatz erreicht einen frühen klinischen Meilenstein
Eine erste klinische Studie, veröffentlicht in Nature Medicine, berichtet frühe klinische Ergebnisse für eine mit CRISPR-Cas9 editierte allogene hämatopoetische Zelltransplantation, die für Patienten mit Hochrisiko- akuter myeloischer Leukämie und myelodysplastischem Syndrom entwickelt wurde. Die Behandlungsstrategie verwendet Spenderzellen, denen das CD33-Ziel entfernt wurde, sodass Ärztinnen und Ärzte die Transplantation mit dem CD33-gerichteten Medikament Gemtuzumab Ozogamicin fortsetzen können, ohne normale, vom Spender stammende myeloische Zellen demselben Risikoniveau auszusetzen.
Die Logik hinter dem Ansatz ist einfach, technisch jedoch ambitioniert. Patienten mit Hochrisiko-AML oder MDS können selbst nach einer allogenen hämatopoetischen Zelltransplantation rezidivieren. Eine Herausforderung bei der Erhaltungstherapie nach der Transplantation besteht darin, dass Behandlungen, die verbliebene Leukämie unterdrücken oder beseitigen sollen, auch gesunde Spenderzellen schädigen können. Das Prüfpräparat in dieser Studie, tremtelectogene empogeditemcel, oder trem-cel, soll einen Teil dieses Problems lösen, indem CD33 vor der Infusion aus dem Spendertransplantat entfernt wird.
Was die Phase-1/2a-Studie ergab
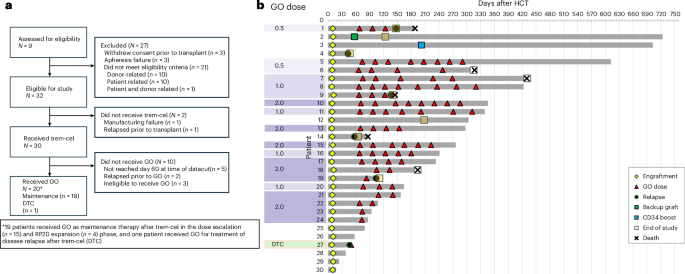
Die multizentrische, offene Phase-1/2a-Studie schloss erwachsene Patienten mit AML oder MDS ein, bei denen ein hohes Rückfallrisiko angenommen wurde. Nach myeloablativer Konditionierung erhielten die Patienten trem-cel. Einige Teilnehmende erhielten anschließend eine Erhaltungstherapie mit Gemtuzumab Ozogamicin in 28-Tage-Zyklen bei Dosen von 0,5 mg/m2 bis 2,0 mg/m2.
Der primäre Sicherheitsendpunkt war die neutrophile Engraftment bis Tag 28. Laut dem veröffentlichten Bericht erfüllten alle 30 Patienten, die trem-cel erhielten, diesen Endpunkt. Die mediane Zeit bis zur neutrophilen Engraftment betrug 10 Tage, mit einem 95%-Konfidenzintervall von 9 bis 10 Tagen. Das ist wichtig, weil verzögerte oder ausbleibende Engraftment eines der zentralen Risiken jeder Transplantationsstrategie ist, besonders bei einer, die genomeditierte Spenderzellen einsetzt.
Neunzehn Patienten erhielten eine posttransplantative Erhaltung mit Gemtuzumab Ozogamicin, darunter 15 im Phase-1-Dosis-Eskalationsteil und vier in der Phase-2-Dosisexpansion. Die Studie berichtet, dass Gemtuzumab Ozogamicin bis zur empfohlenen Phase-2-Dosis von 2 mg/m2 sicher vertragen wurde. Das Papier merkt außerdem an, dass die Studie vorzeitig beendet wurde und als Abschlussbericht einschließlich des abgeschlossenen Phase-1-Teils dient.