Eine neue Grenze in der Krebsbehandlung
Krebsimpfstoffe nehmen eine einzigartige Position in der Medizingeschichte ein: ein therapeutisches Konzept, das über ein Jahrhundert lang verfolgt wurde, aber erst kürzlich die biologischen Erkenntnisse und technologischen Werkzeuge erlangte, um es auf klinisch bedeutsame Weise funktionsfähig zu machen. Eine umfassende Übersicht, die in Nature Medicine veröffentlicht wurde, untersucht den derzeitigen Stand des Feldes und verfolgt den Weg von frühen Rückschlägen zu den raffinierten mRNA- und Neoantigen-fokussierten Ansätzen, die nun mit echten Erfolgsaussichten durch klinische Studien voranschreiten.
Der Zeitpunkt der Übersicht spiegelt echte Beschleunigung im Feld wider. Die mRNA-Technologieplattformen, die COVID-19-Impfstoffe angetrieben haben, wurden mit bemerkenswerter Geschwindigkeit an Krebsanwendungen angepasst, und frühe klinische Daten aus personalisierten Krebsimpfstoffprogrammen waren ermutigend genug, um Milliarden an Investitionen von Pharmaunternehmen anzuziehen, die Jahre lang skeptisch gegenüber der kommerziellen Rentabilität von Krebsimpfungen waren. Die Landschaft 2026 unterscheidet sich grundlegend von der vor nur fünf Jahren.
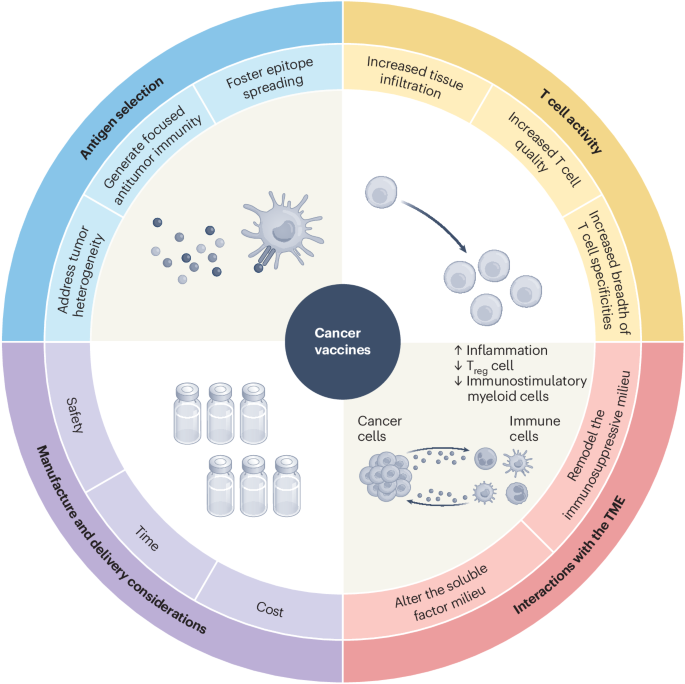
Krebsimpfstoffe funktionieren nach einem anderen Prinzip als traditionelle Impfstoffe gegen Infektionskrankheiten. Anstatt das Immunsystem zu trainieren, um einen Krankheitserreger vor der Exposition zu erkennen, zielen Krebsimpfstoffe darauf ab, das Immunsystem zu trainieren, bereits vorhandene Tumorzellen zu erkennen und zu zerstören. Dieser therapeutische Impfansatz erfordert eine genaue Identifizierung der molekularen Ziele auf Tumorzellen, die sie als fremd kennzeichnen, und die Erzeugung einer starken Immunantwort, um die immunsuppressive Umgebung zu überwinden, die Tumoren schaffen, um sich vor Immunbeseitigung zu schützen.
Personalisierte mRNA-Krebsimpfstoffe
Der wissenschaftlich fortschrittlichste Krebsimpfstoffansatz in der aktuellen klinischen Entwicklung nutzt mRNA-Technologie, um personalisierte Impfstoffe zu entwickeln, die auf Neoantigene abzielen - mutierte Proteinbruchstücke, die für den Tumor eines einzelnen Patienten einzigartig sind. Da diese Ziele durch spezifische Mutationen in den Krebszellen jedes Patienten entstehen, sind sie nicht in normalem Gewebe vorhanden und machen sie zu hochselektiven Zielen für Immunangriff.
Der Personalisierungsprozess der Impfstoffentwicklung umfasst die Sequenzierung des Tumors eines Patienten zur Identifizierung seiner spezifischen Mutationen, die Verwendung von Rechentools zur Vorhersage, welche mutierten Peptide auf Tumorzellenflächen angezeigt und von Immunzellen erkannt werden, die Synthese eines mRNA-Impfstoffs, der diese Ziele kodiert, und die Verabreichung des Impfstoffs zur Stimulierung einer Immunantwort. Die gesamte Pipeline vom Tumor-Sequencing bis zur Impfstoffverabreichung dauert jetzt in fortgeschrittenen Produktionsumgebungen Wochen, was nur wenige Jahre zuvor Monate brauchte.
Moderna und Merck haben die klinische Entwicklung in diesem Bereich mit ihrem Kandidaten mRNA-4157 angeführt, der in Kombination mit dem Checkpoint-Inhibitor pembrolizumab in einer randomisierten Phase-2-Studie eine statistisch signifikante Reduktion des Melanom-Rezidivs zeigte - ein Ergebnis, das das Feld elektrisierte und seitdem zur Expansion in mehrere Krebstypen führte. Die Nature Medicine-Übersicht ordnet dieses Ergebnis im Kontext eines breiteren Feldes ein, das jetzt personalisierte mRNA-Impfstoffe über Lungen-, Darm-, Blasen- und andere Krebsarten evaluiert.
Shared-Antigen-Impfstoffe und Kombinationsansätze
Nicht alle Krebsimpfstoffprogramme sind personalisiert. Shared-Antigen-Impfstoffe zielen auf überexprimierte Proteine in vielen Patiententumoren ab - Ziele wie HER2, MAGE und tumorassoziierte Kohlenhydratantigene, die häufig genug sind, um die Entwicklung von Produkten auf Lager mit potenziell einfacherer Herstellung und niedrigerem Preis zu unterstützen. Diese Ansätze tauschen einen Teil der Spezifität personalisierter Neoantigene gegen die praktischen Vorteile skalierbare Produktion und standardisierte klinische Entwicklung.
Kombinationsansätze, die Krebsimpfstoffe mit Checkpoint-Inhibitoren, CAR-T-Therapien oder anderen Immuntherapie-Modalitäten verbinden, sind zu einem Hauptuntersuchungsbereich geworden. Der Grund ist, dass Impfstoffe tumorspezifische Immunantworten verstärken, während Checkpoint-Inhibitoren die Bremsen entfernen, die Tumoren nutzen, um diese Antworten zu unterdrücken - was potenziell synergistische Anti-Tumor-Aktivität erzeugt, die kein Ansatz allein erreicht. Klinische Daten aus diesen Kombinationen sammeln sich über mehrere Tumortypen hinweg an.
Die Übersicht hebt die zunehmende Raffinesse von Impfstoffverabreichungssystemen hervor, einschließlich optimierter Lipid-Nanopartikel für Tumor-Antigen-Präsentation, neuartige Adjuvans-Formulierungen, die Immunaktivierung ohne übermäßige Toxizität verstärken, und in-vivo-programmierbare Ansätze, die personalisierte Immunantworten unter Verwendung endogener zellulärer Maschinerie anstelle von Ex-vivo-Herstellungsschritten erzeugen.
Herausforderungen und offene Fragen
Trotz echtem Fortschritt steht sich das Krebsimpfstofffeld erheblichen Herausforderungen gegenüber, die die Nature Medicine-Übersicht direkt behandelt. Tumor-Immunflucht - die Fähigkeit von Krebszellen, die Antigenexpression herabzuregulieren, immunsuppressive Mikroumgebungen zu schaffen und Resistenz gegen Immunangriff zu entwickeln - bleibt ein grundlegendes Hindernis. Impfstoffe, die starke anfängliche Immunantworten erzeugen, können dennoch nicht zu dauerhafter Tumorkontrolle führen, wenn der Tumor die von ihnen stimulierte Immunantwort zu umgehen entwickelt.
Die Patientenauswahl bleibt unvollständig verstanden. Einige Tumortypen und einige Patienten scheinen dramatisch auf Krebsimpfstoffansätze zu reagieren, während andere minimalen Vorteil zeigen, und die biologischen Prädiktoren der Reaktion sind noch nicht gut genug charakterisiert, um Behandlungsentscheidungen mit Vertrauen zu leiten. Die Identifizierung von Biomarkern, die die Impfstoffreaktion vorhersagen, ist eine große Forschungspriorität über das gesamte Feld hinweg.
Herstellungskosten und -komplexität, besonders für personalisierte Impfstoffe, bleiben ein Hindernis für breiten Zugang. Der Prozess der Tumor-Sequenzierung, Zielidentifikation, Entwurf und Synthese eines individualisierten Impfstoffs sowie Verabreichung innerhalb eines klinisch bedeutsamen Zeitrahmens beinhaltet beträchtliche Infrastruktur und bleibt teuer. Die Senkung dieser Kosten durch Prozessinnovation und Produktionsmaßstab wird notwendig sein, damit personalisierte Krebsimpfstoffe ihr volles Patientenpotenzial erreichen.
Der Weg nach vorne
Die Nature Medicine-Übersicht schließt mit gemäßigtem Optimismus über die Flugbahn des Feldes ab. Mehrere Phase-3-Studien laufen jetzt für Krebsimpfstoffkandidaten in Umgebungen, in denen Phase-2-Daten ausreichend überzeugend waren, um die Investition zu rechtfertigen. Ergebnisse aus diesen größeren Studien werden in den kommenden Jahren ankommen und werden maßgeblich bestimmen, wie schnell Krebsimpfstoffe von experimenteller zu Standard-Versorgungsbehandlung in der Onkologie-Praxis übergehen.
Die Konvergenz von mRNA-Plattformtechnologie, KI-gestützter Neoantigen-Vorhersage, schneller Tumor-Sequenzierung und zunehmend ausgefeiltem Verständnis der Tumor-Immunologie hat die Bedingungen geschaffen, unter denen Krebsimpfungen auf Weise erfolgreich sind, die frühere Generationen von Forschern nicht erreichen konnten. Ob das Feld letztendlich das Versprechen einlösen wird, das Immunsystem in eine breit anwendbare Krebsbehandlung umzuwandeln, bleibt abzuwarten, aber die klinischen Beweise sind jetzt stark genug, um diese Möglichkeit ernst zu nehmen.
Dieser Artikel basiert auf Berichten von Nature Medicine. Lesen Sie den ursprünglichen Artikel.