基因编辑移植方法达到早期临床里程碑
发表在 Nature Medicine 上的一项首次人体研究报告了 CRISPR-Cas9 编辑的异基因造血细胞移植的早期临床结果,该方案面向高风险急性髓系白血病和骨髓增生异常综合征患者。该治疗策略使用去除了 CD33 靶点的供体细胞,使医生能够在移植后使用 CD33 定向药物吉妥珠单抗奥唑米星,而不会让正常的供体来源髓系细胞暴露于同等程度的风险之中。
这一方法背后的逻辑简单,但技术上极具挑战。高风险 AML 或 MDS 患者即便接受异基因造血细胞移植后,仍可能复发。移植后维持治疗的一项难点在于,用于抑制或清除残余白血病的疗法也可能损伤健康的供体细胞。本试验中的研究性产品 tremtelectogene empogeditemcel,即 trem-cel,旨在通过在输注前删除供体移植物中的 CD33 来解决这一问题的一部分。
1/2a 期试验发现了什么
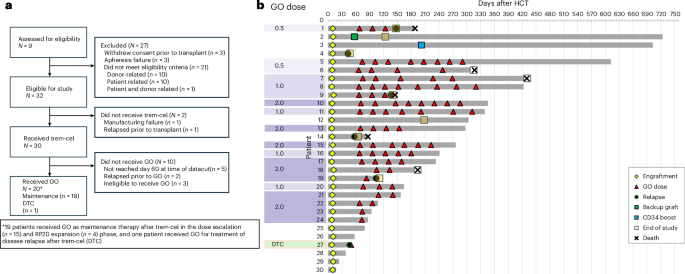
这项多中心、开放标签的 1/2a 期研究招募了被认为具有高复发风险的 AML 或 MDS 成年患者。在接受清髓性预处理后,患者接受 trem-cel。随后,部分受试者进入吉妥珠单抗奥唑米星维持治疗阶段,按 28 天一个周期给药,剂量范围为 0.5 mg/m2 至 2.0 mg/m2。
主要安全性终点是截至第 28 天的中性粒细胞植入。根据已发表报告,接受 trem-cel 的 30 名患者全部达到该终点。中性粒细胞植入的中位时间为 10 天,95% 置信区间为 9 至 10 天。这一点很重要,因为植入延迟或失败是任何移植策略中的核心风险之一,在基因编辑供体细胞方案中尤为如此。
共有 19 名患者接受了移植后的吉妥珠单抗奥唑米星维持治疗,其中 15 名来自第 1 期剂量递增部分,4 名来自第 2 期剂量扩展部分。研究报告称,吉妥珠单抗奥唑米星在推荐的第 2 期剂量 2 mg/m2 下可安全耐受。论文还指出,该试验已提前结束,并作为已完成第 1 期部分的最终报告。
为什么 CD33 在这一疾病场景中重要
CD33 是包括 AML 在内的髓系恶性肿瘤中公认的治疗靶点,但它同样也表达于正常髓系细胞上。这种重叠正是移植后进行 CD33 靶向维持治疗之所以困难的原因之一:标记白血病细胞的同一抗原,也会标记医生试图重建的供体来源造血系统。通过在移植前从供体造血细胞中去除 CD33,研究人员试图创造一种既能保持功能,又不易受到后续 CD33 定向治疗伤害的移植物。
如果这一概念在更大规模研究中站得住脚,它可能指向一种更广泛的移植肿瘤学模式:先编辑供体移植物,再在移植后更积极地使用靶向药物。换句话说,这种细胞疗法不只是为了替换病变骨髓。它也旨在重新定义移植后的维持治疗能够做到什么。
哪些地方令人鼓舞,哪些问题仍未解决
报告中最令人鼓舞的部分是,这种编辑后的移植物似乎跨过了一个基础但关键的临床门槛。30 名接受治疗患者在第 28 天全部实现中性粒细胞植入,这强烈表明该编辑产品能够按临床医生预期的时间表重建髓系恢复。维持性吉妥珠单抗奥唑米星在推荐的第 2 期剂量下可耐受,也进一步支持了通过保护供体细胞免受靶向毒性影响这一生物学前提。
与此同时,这仍是一项早期研究,患者数量有限。文章摘要提到的其他次要终点包括移植物抗宿主病、移植物失败、移植相关死亡、CD33 阴性髓系细胞比例以及生存情况,但所提供的来源文本仅对这些结局给出了部分视角。因此,最稳妥的结论不是该策略已经解决了复发风险,而是它在一个两方面都很难取得进展的场景中,证明了可行性并显示出早期安全信号。
基因编辑在移植领域的一项值得注意的进展
血液疾病中的基因编辑过去常被放在自体细胞疗法的框架下讨论,即患者自身细胞被修饰后再回输。这项试验则聚焦于一种面向移植患者、用于侵袭性疾病的异基因产品。这使它不仅对 AML 有意义,也具有更广泛的价值。它表明,CRISPR 基因编辑不仅可能用于纠正遗传缺陷,还可能用于工程化供体移植物,使其成为更具韧性的治疗平台。
就目前而言,这项研究更像是一个概念验证里程碑,而不是能改变临床实践的结果。但对于高风险 AML 和 MDS 来说,移植后复发仍是该领域最难解决的问题之一;一个专门设计来承受靶向维持治疗的移植产品,无疑是一个严肃的思路。本周发表的早期临床记录表明,这一思路已经从理论走向了真实、尽管仍然初步的患者体验。
本文依据 Nature Medicine 的报道。阅读原文。
Originally published on nature.com