மரபணு-திருத்தப்பட்ட மாற்று அணுகுமுறை ஆரம்ப மருத்துவ மைல்கல்லை எட்டுகிறது
Nature Medicine-இல் வெளியான முதல் மனித ஆய்வு, உயர் ஆபத்து acute myeloid leukemia மற்றும் myelodysplastic syndrome உடைய நோயாளிகளுக்காக வடிவமைக்கப்பட்ட CRISPR-Cas9-திருத்தப்பட்ட allogeneic hematopoietic cell transplant-ற்கான ஆரம்ப மருத்துவ முடிவுகளை அறிவிக்கிறது. இந்த சிகிச்சைத் திட்டம், CD33 இலக்கை நீக்கிய donor cells-ஐ பயன்படுத்துகிறது; இதனால் மருத்தவர்கள் சாதாரண donor-derived myeloid cells-ஐ அதே அளவு ஆபத்துக்குள்ளாக்காமல், transplantation-க்குப் பிறகு CD33-directed மருந்தான gemtuzumab ozogamicin-ஐ தொடர்ச்சியாக வழங்க முடிகிறது.
இந்த அணுகுமுறையின் தர்க்கம் நேர்மையானது, ஆனால் தொழில்நுட்ப ரீதியாக மிகுந்த சவாலானது. உயர் ஆபத்து AML அல்லது MDS கொண்ட நோயாளிகள் allogeneic hematopoietic cell transplantation செய்த பிறகும் மீண்டும் நோய் வரக்கூடும். post-transplant maintenance-இல் உள்ள சவால்களில் ஒன்று, மீதமுள்ள leukemia-வை அடக்க அல்லது அழிக்க நோக்கமுள்ள சிகிச்சைகள் ஆரோக்கிய donor cells-ஐயும் சேதப்படுத்தலாம் என்பதே. இந்த சோதனையில் ஆய்வுக்குரிய தயாரிப்பான tremtelectogene empogeditemcel, அல்லது trem-cel, infusion-க்கு முன் donor graft-இல் இருந்து CD33-ஐ நீக்குவதன் மூலம் இந்தப் பிரச்சினையின் ஒரு பகுதியைத் தீர்க்கும் நோக்கம் கொண்டது.
phase 1/2a சோதனையில் என்ன கண்டுபிடிக்கப்பட்டது
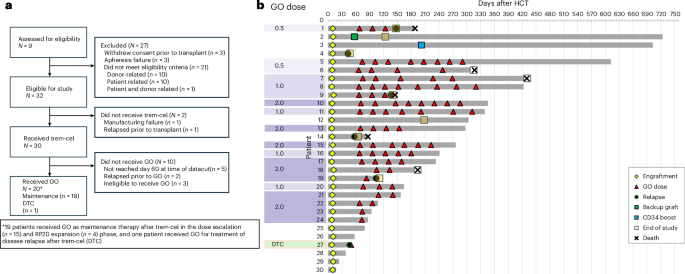
பல மையங்களில் நடைபெற்ற, open-label phase 1/2a ஆய்வில், மீள்நோய் ஆபத்து அதிகமாகக் கருதப்பட்ட AML அல்லது MDS கொண்ட பெரியவர்கள் சேர்க்கப்பட்டனர். myeloablative conditioningக்குப் பிறகு, நோயாளிகள் trem-cel பெற்றனர். பின்னர் சிலர் 28 நாள் சுழற்சிகளில் 0.5 mg/m2 முதல் 2.0 mg/m2 வரையான அளவுகளில் maintenance gemtuzumab ozogamicin பெற்றனர்.
முதன்மை பாதுகாப்பு முடிவுக்குறி 28ஆம் நாளுக்குள் neutrophil engraftment ஆகும். வெளியிடப்பட்ட அறிக்கையின்படி, trem-cel பெற்ற 30 நோயாளிகளும் அந்த முடிவுக்குறியை அடைந்தனர். neutrophil engraftment-க்கு நடுத்தர காலம் 10 நாட்கள்; 95% நம்பகத்தன்மை இடைவெளி 9 முதல் 10 நாட்கள். இது முக்கியமானது, ஏனெனில் தாமதமான அல்லது தோல்வியுற்ற engraftment என்பது எந்த transplant முறையிலும், குறிப்பாக genome-edited donor cells உள்ள முறையில், மைய ஆபத்துகளில் ஒன்றாகும்.
19 நோயாளிகள் post-transplant gemtuzumab ozogamicin maintenance பெற்றனர்; இதில் 15 பேர் phase 1 dose-escalation பகுதியில், 4 பேர் phase 2 dose expansion பகுதியில் இருந்தனர். ஆய்வு, gemtuzumab ozogamicin recommended phase 2 dose ஆன 2 mg/m2 வரை பாதுகாப்பாகத் தாங்கப்பட்டதாக தெரிவிக்கிறது. மேலும் அந்த சோதனை முன்கூட்டியே நிறுத்தப்பட்டு, முடிக்கப்பட்ட phase 1 பகுதியை உள்ளடக்கிய இறுதி அறிக்கையாக இருப்பதாகவும் paper குறிப்பிடுகிறது.