Uma abordagem de transplante editada geneticamente atinge um marco clínico inicial
Um estudo de primeira em humanos publicado em Nature Medicine relata resultados clínicos iniciais de um transplante alogênico de células hematopoéticas editado com CRISPR-Cas9, desenvolvido para pacientes com leucemia mieloide aguda de alto risco e síndrome mielodisplásica. A estratégia de tratamento usa células do doador das quais o alvo CD33 foi removido, permitindo que os médicos sigam o transplante com o medicamento direcionado a CD33 gemtuzumabe ozogamicina sem expor as células mieloides normais derivadas do doador ao mesmo nível de risco.
A lógica por trás da abordagem é direta, mas tecnicamente ambiciosa. Pacientes com LMA ou SMD de alto risco podem recidivar mesmo após o transplante alogênico de células hematopoéticas. Um desafio na manutenção pós-transplante é que terapias destinadas a suprimir ou eliminar a leucemia residual também podem danificar células saudáveis do doador. O produto investigacional deste ensaio, tremtelectogene empogeditemcel, ou trem-cel, pretende resolver parte desse problema ao حذف CD33 do enxerto do doador antes da infusão.
O que o ensaio de fase 1/2a encontrou
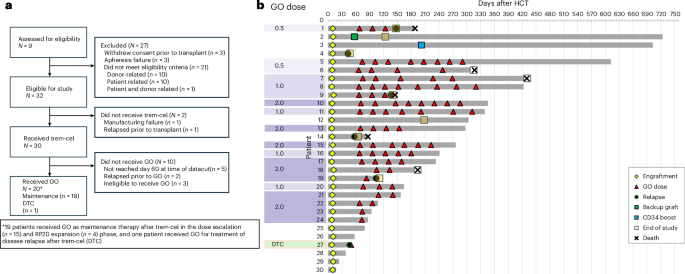
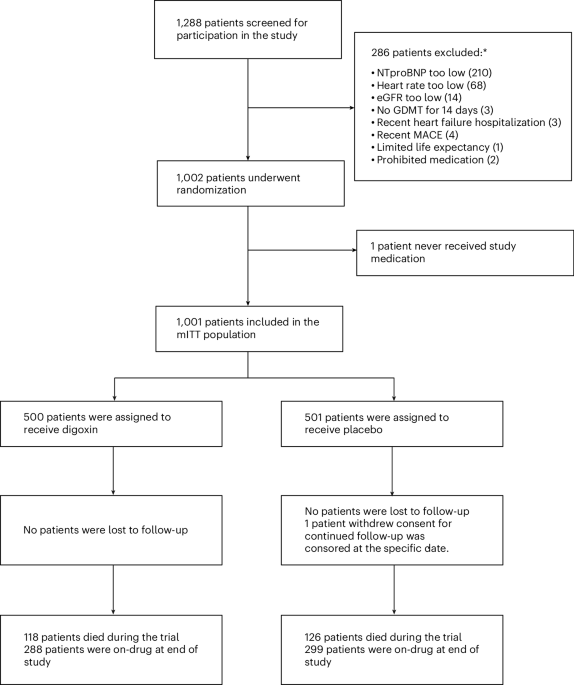
O estudo multicêntrico e aberto de fase 1/2a incluiu pacientes adultos com LMA ou SMD considerados de alto risco de recaída. Após condicionamento mieloablativo, os pacientes receberam trem-cel. Alguns participantes então passaram a receber manutenção com gemtuzumabe ozogamicina em ciclos de 28 dias, em doses variando de 0,5 mg/m2 a 2,0 mg/m2.
O desfecho primário de segurança foi a enxertia de neutrófilos até o dia 28. Segundo o relatório publicado, todos os 30 pacientes que receberam trem-cel atingiram esse desfecho. O tempo mediano para enxertia de neutrófilos foi de 10 dias, com intervalo de confiança de 95% de 9 a 10 dias. Isso importa porque a enxertia tardia ou fracassada é um dos riscos centrais de qualquer estratégia de transplante, especialmente em uma que envolve células do doador editadas no genoma.
Dezenove pacientes receberam manutenção pós-transplante com gemtuzumabe ozogamicina, incluindo 15 na parte de escalonamento de dose da fase 1 e quatro na expansão de dose da fase 2. O estudo relata que o gemtuzumabe ozogamicina foi tolerado com segurança até a dose recomendada da fase 2 de 2 mg/m2. O artigo também observa que o ensaio foi encerrado precocemente e serve como relatório final, incluindo a parte concluída da fase 1.