Les thérapies géniques sur mesure passent de la théorie à la pratique
Les maladies pédiatriques rares ne sont plus seulement considérées comme des curiosités scientifiques. Dans une nouvelle correspondance publiée dans Nature Medicine, un groupe de chercheurs affirme qu’elles deviennent de plus en plus des candidates pour des thérapies cellulaires et géniques conçues sur mesure, y compris des traitements élaborés pour un seul patient.
Les auteurs soulignent un changement récent frappant. Des troubles héréditaires autrefois pratiquement incurables voient désormais des thérapies géniques administrées en une seule fois produire des bénéfices significatifs et durables. Ce changement est important en soi, mais l’article soutient que la perturbation la plus profonde est structurelle : les régulateurs, les développeurs et les systèmes de santé sont désormais confrontés à des médicaments qui ne correspondent pas aux hypothèses du développement pharmaceutique conventionnel.
Selon la correspondance, les essais menés chez un seul patient ne sont plus hypothétiques. Les auteurs citent une maladie neurologique ultra-rare dans laquelle une thérapie génique à base de virus adéno-associé, adaptée au patient, a été développée et administrée en trois ans. Ils mettent aussi en avant un cas encore plus rapide, dans lequel une thérapie d’édition de base propre à un patient a été créée, validée par les autorités de régulation et administrée à un nouveau-né atteint d’un trouble métabolique mortel en environ huit mois.
Ces exemples suggèrent que la partie scientifique et manufacturière de la thérapie individualisée progresse rapidement. Le problème le plus difficile, avancent les auteurs, consiste à construire une voie qui permette de rendre ces traitements accessibles à davantage d’enfants, plutôt qu’à quelques cas extraordinaires seulement.
Le problème d’accès est désormais aussi économique que scientifique
La correspondance présente l’accès comme le principal goulot d’étranglement. Alors que les thérapies géniques personnalisées deviennent plus réalisables, la plupart des enfants atteints de maladies rares n’ont toujours pas accès à un traitement efficace. L’article ne décrit pas cet écart comme un échec purement scientifique. Il soutient plutôt que le modèle commercial classique des médicaments est mal adapté à des thérapies hautement individualisées.
Ce décalage est déjà visible sur le marché. Les auteurs notent que les entreprises de biotechnologie qui ont contribué à ouvrir la voie aux thérapies géniques ont eu du mal à rester commercialement viables et, dans certains cas, ont retiré des produits malgré leur efficacité vitale. Autrement dit, la question n’est pas seulement de savoir si une thérapie peut fonctionner. Il s’agit de savoir si les institutions chargées de financer, d’approuver, de fabriquer et de soutenir les traitements peuvent prendre en charge des produits destinés à des populations de patients extrêmement réduites, voire à un seul enfant.
Cela crée une contradiction au cœur du domaine. Plus une thérapie est précisément adaptée, moins elle ressemble au type de produit évolutif que le modèle pharmaceutique traditionnel à but lucratif est conçu pour récompenser. Pour les maladies fréquentes, de grands essais et de vastes marchés peuvent justifier des années d’investissement. Pour les troubles pédiatriques ultra-rares, ce même modèle peut devenir un obstacle plutôt qu’un moteur.
La correspondance soutient que, si le système ne change pas, les thérapies individualisées pourraient continuer à apparaître comme des percées isolées plutôt que comme une catégorie de traitement fiable.
Un cadre destiné à relier développement et réglementation
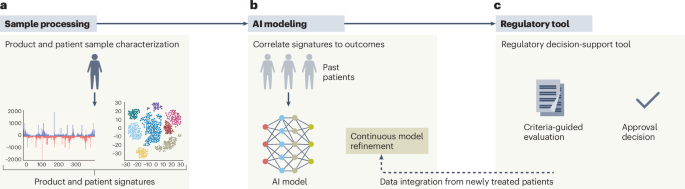
L’article présente ce qu’il appelle le cadre UNICORN, présenté comme une voie allant de la caractérisation du produit à la décision réglementaire. L’extrait de la correspondance fourni ici ne détaille pas tous les aspects opérationnels de ce cadre, mais son objectif est clair d’après l’argument des auteurs : créer une structure reproductible pour évaluer les thérapies géniques sur mesure sans les forcer à entrer dans des voies d’approbation conçues pour des médicaments de grande diffusion.
Cela compte parce que le modèle standard dépend fortement de grands cohortes, de lots de fabrication reproductibles et d’une validation commerciale étendue. Les thérapies pédiatriques ultra-rares peuvent ne présenter aucune de ces caractéristiques. Un régulateur doit toujours évaluer la qualité, la sécurité et le bénéfice probable, mais le dossier de preuves peut devoir prendre une forme différente lorsque le traitement est conçu autour de la mutation, du calendrier et de la trajectoire clinique d’un seul enfant.
La correspondance pointe donc vers un modèle plus adaptable, capable de relier la caractérisation du produit et l’examen réglementaire d’une manière qui préserve la rigueur tout en reconnaissant que les thérapies individualisées sont fondamentalement des produits différents.
Le message sous-jacent n’est pas qu’il faille affaiblir les normes. C’est qu’elles devront peut-être être traduites dans un nouveau format. Si une thérapie est fabriquée pour un patient, la logique d’approbation ne peut pas reposer sur les mêmes hypothèses que celles utilisées pour un produit destiné à des dizaines de milliers de personnes.
Pourquoi la maladie rare pédiatrique est le point de pression
La maladie rare pédiatrique est l’endroit où cette pression est la plus aiguë. Les patients sont peu nombreux, la progression peut être rapide et les délais peuvent avoir des conséquences à vie. Les deux exemples cités par les auteurs soulignent cette urgence. Un délai de développement de trois ans pour une thérapie personnalisée est déjà exceptionnellement compressé selon les standards historiques du développement du médicament. Un parcours de huit mois entre la conception, l’autorisation réglementaire et le traitement chez un nouveau-né est encore plus remarquable.
Ces calendriers montrent à la fois la promesse et la fragilité du domaine. Ils démontrent que les thérapies sur mesure peuvent avancer à une vitesse remarquable lorsque la science, la fabrication, la réglementation et le besoin clinique s’alignent. Ils posent aussi une question difficile : si cela peut se produire dans des cas exceptionnels, que faudrait-il pour que cela se produise de manière systématique ?
La correspondance soutient que la réponse n’est pas seulement davantage d’innovation en laboratoire. C’est aussi une meilleure conception institutionnelle. Les maladies rares pédiatriques n’ont souvent pas de traitement de secours ni de grand marché commercial. Cela en fait un cas d’essai pour savoir si la médecine peut bâtir des systèmes de développement autour du besoin plutôt que de l’échelle.
Ce que cette proposition signale pour le domaine
L’importance de l’article tient moins à l’annonce d’une thérapie unique qu’à la reconnaissance qu’une nouvelle catégorie de médicament arrive plus vite que les systèmes hérités ne peuvent l’absorber. Les auteurs décrivent un monde dans lequel les thérapies géniques sur mesure deviennent techniquement possibles, cliniquement pertinentes et pourtant structurellement difficiles à délivrer.
Si leur argument est juste, les progrès futurs dans les maladies pédiatriques rares dépendront non seulement de meilleurs vecteurs, outils d’édition ou méthodes de fabrication, mais aussi de voies d’approbation qui reconnaissent les thérapies individualisées comme une réalité durable. La correspondance affirme que la médecine des maladies rares est déjà entrée dans cette phase.
C’est un changement important. Pendant des années, la thérapie génique personnalisée ressemblait souvent à une ambition de frontière. Les exemples cités ici suggèrent qu’elle devient désormais autant un défi administratif et réglementaire qu’un défi scientifique. Les prochaines percées pourraient dépendre de la capacité des régulateurs et des développeurs à transformer des succès ponctuels en un système viable.
Pour les familles confrontées à des troubles infantiles dévastateurs, cette distinction n’est pas abstraite. Elle pourrait déterminer si la médecine sur mesure reste l’exception, ou commence à faire partie des soins courants pour des maladies trop rares pour correspondre à l’ancien modèle.
Cet article s’appuie sur un reportage de Nature Medicine. Lire l’article original.
Originally published on nature.com