Une option orale de relais pour un problème bien connu de l’obésité
L’une des parties les plus difficiles du traitement de l’obésité n’est pas de perdre du poids au départ, mais de conserver ces gains lorsque le traitement change ou s’arrête. Une nouvelle étude de phase 3b publiée dans
Nature Medicine
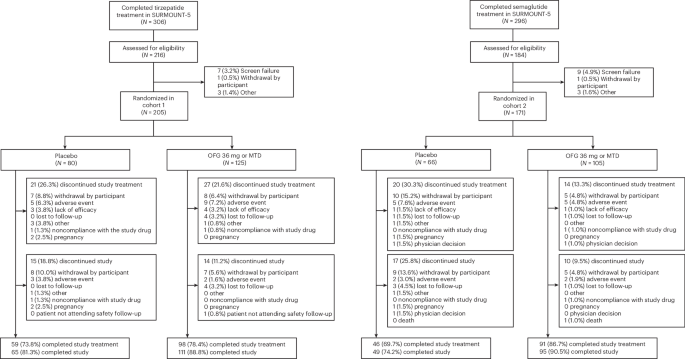
s’attaque directement à ce problème de maintien, en testant si un agoniste oral du récepteur GLP-1 pris une fois par jour peut aider les personnes à préserver la perte de poids déjà obtenue grâce à des médicaments injectables.Le médicament est l’orforglipron, un agoniste oral non peptidique du récepteur GLP-1. Dans l’essai ATTAIN-MAINTAIN récemment publié, les chercheurs ont recruté des personnes déjà traitées par tirzépatide ou sémaglutide dans l’étude SURMOUNT-5. Les participants ont ensuite été randomisés, selon un schéma en double aveugle et contrôlé par placebo, pour recevoir soit de l’orforglipron oral quotidien, soit un placebo.
La question centrale était pratique et cliniquement importante : une fois qu’un patient atteint un plateau de poids sous traitement injectable, un médicament oral peut-il l’aider à conserver une plus grande partie de cette perte au cours de l’année suivante ?
Ce que l’essai a montré
La réponse, d’après cette étude, est oui. Parmi les participants du groupe ayant déjà reçu du tirzépatide et ayant atteint un plateau pondéral, ceux assignés à l’orforglipron ont conservé, selon une estimation fondée sur un modèle, 74,7 % de leur réduction pondérale à la semaine 52. Le groupe placebo a conservé 49,2 %. Cela a donné une différence de traitement estimée à 25,5 points de pourcentage, avec une valeur de P rapportée inférieure à 0,001.
Les résultats étaient également solides dans le groupe ayant déjà reçu du sémaglutide. Les participants sous orforglipron ont conservé, selon une estimation fondée sur un modèle, 79,3 % de leur perte de poids à la semaine 52, contre 37,6 % pour le placebo. La différence de traitement estimée était de 41,7 points de pourcentage, là encore avec P < 0,001.
L’article indique que tous les critères de jugement secondaires clés ont également été atteints, même si le résumé ne détaille pas chacun d’eux individuellement. Il rapporte aussi des améliorations des facteurs de risque cardiométaboliques et un profil de sécurité globalement comparable à celui des agonistes injectables du récepteur GLP-1.
Les événements indésirables les plus fréquents étaient gastro-intestinaux, décrits le plus souvent comme légers à modérés. Ce point importe, car la tolérance détermine souvent si un traitement peut fonctionner en dehors d’essais strictement contrôlés.