Une approche de greffe modifiée génétiquement franchit une première étape clinique
Une étude de première administration chez l’humain publiée dans Nature Medicine rapporte les premiers résultats cliniques d’une greffe allogénique de cellules hématopoïétiques éditée par CRISPR-Cas9, conçue pour des patients atteints de leucémie aiguë myéloïde à haut risque et de syndrome myélodysplasique. La stratégie thérapeutique utilise des cellules donneuses dont la cible CD33 a été supprimée, ce qui permet aux médecins d’enchaîner avec le médicament ciblant CD33, le gemtuzumab ozogamicin, sans exposer les cellules myéloïdes normales d’origine donneuse au même niveau de risque.
La logique de cette approche est simple, mais techniquement ambitieuse. Les patients atteints de LAM ou de SMD à haut risque peuvent rechuter même après une greffe allogénique de cellules hématopoïétiques. L’un des défis du traitement d’entretien post-greffe est que les thérapies destinées à supprimer ou éliminer la leucémie résiduelle peuvent aussi endommager les cellules saines du donneur. Le produit expérimental de cet essai, tremtelectogene empogeditemcel, ou trem-cel, vise à résoudre une partie de ce problème en supprimant CD33 du greffon donneur avant la perfusion.
Ce qu’a montré l’essai de phase 1/2a
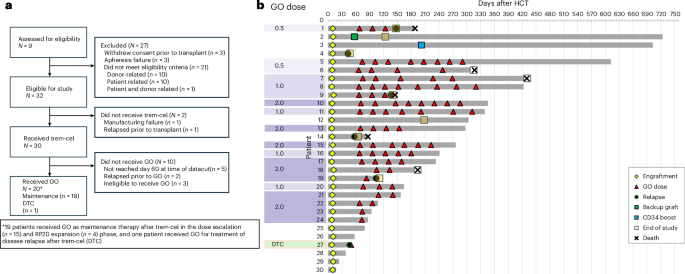
L’étude multicentrique en ouvert de phase 1/2a a recruté des patients adultes atteints de LAM ou de SMD considérés comme présentant un risque élevé de rechute. Après un conditionnement myéloablatif, les patients ont reçu trem-cel. Certains participants ont ensuite reçu un entretien par gemtuzumab ozogamicin en cycles de 28 jours, à des doses allant de 0,5 mg/m2 à 2,0 mg/m2.
Le critère principal de sécurité était la prise de greffe des neutrophiles au jour 28. Selon le rapport publié, les 30 patients ayant reçu trem-cel ont atteint ce critère. Le délai médian de prise de greffe des neutrophiles était de 10 jours, avec un intervalle de confiance à 95 % de 9 à 10 jours. C’est important, car la prise de greffe retardée ou échouée constitue l’un des risques centraux de toute stratégie de greffe, en particulier lorsqu’elle implique des cellules donneuses modifiées par génie génétique.
Dix-neuf patients ont reçu un entretien post-greffe par gemtuzumab ozogamicin, dont 15 dans la partie d’escalade de dose de phase 1 et quatre dans l’expansion de dose de phase 2. L’étude indique que le gemtuzumab ozogamicin a été bien toléré jusqu’à la dose recommandée de phase 2 de 2 mg/m2. L’article précise aussi que l’essai a été interrompu plus tôt que prévu et constitue le rapport final, incluant la partie achevée de phase 1.