বড় প্রশ্নের জন্য ছোট এক বর্ণমালা
বিজ্ঞানের সবচেয়ে কঠিন সমস্যাগুলোর একটি একই সঙ্গে সবচেয়ে পুরোনোও: প্রাথমিক পৃথিবীতে জড় রসায়ন কীভাবে জীববিজ্ঞানে রূপ নিল। Universe Today-এ আলোচিত একটি নতুন পর্যালোচনাপত্র এই প্রশ্নটিকে আশ্চর্যজনকভাবে বাস্তবমুখী পথে এগিয়ে নিয়ে যায়। আধুনিক প্রোটিনের সমস্ত জটিলতা পুনর্গঠন করার চেষ্টা না করে, গবেষকেরা পরীক্ষা করছেন আরও সরল সংস্করণগুলো প্রাক-জৈব পরিস্থিতিতে ভাঁজ হতে, কাজ করতে এবং টিকে থাকতে পারত কি না।
The borderlands of foldability: lessons from simplified proteins শিরোনামের এবং Trends in Chemistry-এ প্রকাশিত এই প্রবন্ধটি তথাকথিত সরলীকৃত প্রোটিনের ওপর কেন্দ্রীভূত। মূল ধারণাটি সহজ। আধুনিক প্রোটিন 20টি ভিন্ন অ্যামিনো অ্যাসিড দিয়ে গঠিত, কিন্তু প্রাথমিক পৃথিবীতে সম্ভবত সেই পুরো উপকরণ-সেট ছিল না। প্রথম পেপটাইড ও প্রোটিন যদি আরও ছোট একটি অংশবিশেষের নাগালে থাকত, তবে জীবনের উদ্ভব আধুনিক জীবদের প্রয়োজনের তুলনায় অনেক কম জৈবরাসায়নিক তথ্যের ওপর নির্ভর করেই ঘটতে পারত।
আধুনিক জীববিজ্ঞান কেন বিভ্রান্তিকর হতে পারে
আজকের জীবন্ত ব্যবস্থার প্রোটিনগুলো অত্যন্ত জটিল অণু, যাদের আকারই তাদের কাজের কেন্দ্রে। তারা ত্রিমাত্রিক গঠনে ভাঁজ হয়ে অনুঘটন থেকে শুরু করে গাঠনিক সহায়তা পর্যন্ত সবকিছু সম্ভব করে। সেই জটিলতা থেকে পেছনের দিকে তাকালে প্রথম ধাপগুলো কতটা কঠিন হতে হতো, সে সম্পর্কে বিভ্রান্তিকর ধারণা তৈরি হতে পারে।
পর্যালোচনাটি যুক্তি দেয় যে প্রাচীনতম পেপটাইডগুলো সম্ভবত ছোট ও সরল ছিল, এবং এমন অ্যামিনো অ্যাসিড দিয়ে তৈরি ছিল যা পরিবেশে স্বাভাবিকভাবে উপস্থিত ছিল অথবা অত্যন্ত প্রাথমিক বিপাকক্রিয়ায় উৎপন্ন হয়েছিল। গবেষকেরা প্রাচীন প্রোটিনের জীবাশ্ম সরাসরি উদ্ধার করতে পারেন না, কিন্তু প্রবন্ধটি এটিকে পরীক্ষামূলক কাজের জন্য যুক্তিসংগত সূচনা হিসেবে ধরে।
এখানেই আসে “বর্ণমালা হ্রাস”। বিজ্ঞানীরা মানক 20-এর বদলে প্রায় 7 থেকে 14 অ্যামিনো অ্যাসিডের সীমিত বর্ণমালা ব্যবহার করে প্রোটিন পুনর্গঠন করছেন। লক্ষ্য আধুনিক জীববিজ্ঞানের একটি কাঁচা অনুকরণ তৈরি করা নয়। লক্ষ্য হলো দেখা যে আরও সরল একটি রাসায়নিক শব্দভাণ্ডারও কি সুশৃঙ্খল, কার্যকর গঠন তৈরি করতে পারে।
কম উপাদানে ভাঁজ হওয়া
পর্যালোচনায় বর্ণিত ফলাফলগুলো চোখে পড়ার মতো। বিজ্ঞানীরা জটিল নির্মাণ উপাদানের সম্পূর্ণ শ্রেণি বাদ দিয়েও স্থিতিশীল 3D গঠনে ভাঁজ হতে সক্ষম প্রোটিন তৈরি করতে পেরেছেন। অন্যভাবে বললে, প্রোটিন গঠনের জন্য যে স্থাপত্য-যুক্তি প্রয়োজন, তার অনেকটাই আধুনিক অ্যামিনো অ্যাসিডের পূর্ণ সেটের ওপর নির্ভর করে বলে মনে হয় না।
এই ফলাফল গুরুত্বপূর্ণ, কারণ এটি জীবনের উদ্ভবের স্পষ্ট বাধাকে কমিয়ে দেয়। যদি প্রায় দশটি অ্যামিনো অ্যাসিড নিয়ে গঠিত একটি “প্রাক-জৈব” বর্ণমালা গঠিত প্রোটিন শুরু করার জন্য যথেষ্ট হয়, তবে প্রাথমিক পৃথিবীকে আধুনিক প্রোটিন-সমস্যা একসঙ্গে সমাধান করতে হয়নি। কেবল এমনটুকু রসায়ন দরকার ছিল, যা উপকারী রূপে নিজেরাই সংগঠিত হতে পারে এমন অণু তৈরি করতে সক্ষম।
পর্যালোচনাটি এটিকে জীববিজ্ঞানের জন্য প্রয়োজনীয় মূল কাঠামোগুলো আশ্চর্যজনকভাবে সীমিত তথ্য থেকেও সৃষ্টি হতে পারে—এর প্রমাণ হিসেবে উপস্থাপন করে। এটি রসায়ন থেকে জীবনে পূর্ণ রূপান্তর ব্যাখ্যা করে না, তবে ওই ফাঁকের একটি ভয়াবহ মাত্রাকে সংকুচিত করে।
পুরোনো অনুমান পেল পরীক্ষামূলক সমর্থন
মূল লেখাটি 1966 সালের Richard Eck এবং Margaret Dayhoff-এর একটি সুপরিচিত প্রস্তাবের দিকে ইঙ্গিত করে, যেখানে বলা হয়েছিল যে প্রাচীন সমমিত প্রোটিন ছোট, সরল পেপটাইডের পুনরাবৃত্তি ও সংযোজনের মাধ্যমে তৈরি হতে পারে। আধুনিক কাজ এখন কার্যত সেই ধারণাকেই সমর্থন করছে বলে মনে হয়।
গবেষকেরা দেখেছেন যে সরল পেপটাইড “হোমো-অলিগোমারাইজ” করে, অর্থাৎ কার্যকরী সমমিত প্রোটিনে একত্রিত হয়ে যায়। এই ছবি গুরুত্বপূর্ণ, কারণ সমমিতি একটি সম্ভাব্য শর্টকাট দেয়। শুরুতেই দীর্ঘ, অত্যন্ত নিখুঁতভাবে সংকেতায়িত সিকোয়েন্সের প্রয়োজন নাও থাকতে পারে। ছোট মডিউলের পুনরাবৃত্তি দিয়ে সত্যিকারের সক্ষম গঠন তৈরি করা সম্ভব হতে পারত।
এই দৃষ্টিভঙ্গি জীবনের উৎপত্তি গবেষণাকে আরও ধাপে ধাপে এগোনোর একটি মডেল দেয়। এলোমেলো রসায়ন থেকে অত্যন্ত পরিশীলিত প্রোটিনে এক লাফে পৌঁছানোর কল্পনার বদলে বিজ্ঞানীরা দেখতে পারেন কীভাবে ছোট পেপটাইডের বিনয়ী সমাবেশ সময়ের সঙ্গে সঙ্গে কার্যকারিতা জমা করতে পারত।
পরিবেশও যন্ত্রের অংশ হতে পারে
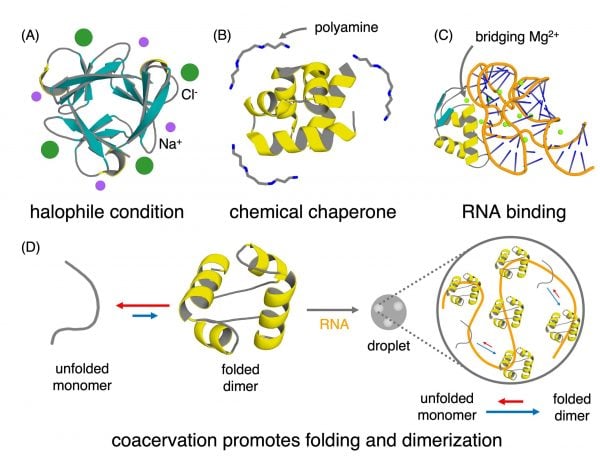
পর্যালোচনাটি আরও জোর দেয় যে প্রাথমিক প্রোটিন একা উদ্ভূত হয়নি। চারপাশের পরিবেশ সেগুলোকে টিকে থাকতে ও ভাঁজ হতে সক্রিয়ভাবে সাহায্য করে থাকতে পারে। এটি দৃষ্টিভঙ্গিতে একটি গুরুত্বপূর্ণ পরিবর্তন। আধুনিক জীববিজ্ঞানে কোষ অভ্যন্তরীণ অবস্থাকে কঠোরভাবে নিয়ন্ত্রণ করে। বিপরীতে, প্রাথমিক পৃথিবীতে খনিজ, লবণ, পৃষ্ঠ এবং স্থানীয় রাসায়নিক পরিবেশ এক ধরনের ভিত্তি বা স্থিতিস্থাপক হিসেবে কাজ করতে পারে।
যদি তা সত্য হয়, তবে প্রথম কার্যকর প্রোটিনগুলো কেবল তাদের অ্যামিনো অ্যাসিড বর্ণমালা ছোট ছিল বলেই সরল ছিল না, বরং পরিবেশও কাজের একটি অংশ করছিল। আধুনিক গবেষণাগারের প্রেক্ষাপটে সীমান্তবর্তী মনে হওয়া কোনো পেপটাইড সহায়ক প্রাক-জৈব নীড়ে সম্পূর্ণ ভিন্নভাবে আচরণ করতে পারত।
এই পরিবেশগত দৃষ্টিভঙ্গি সরলীকৃত প্রোটিন গবেষণার তাৎপর্যকে বিস্তৃত করে। এটি শুধু কোন সিকোয়েন্স তথ্য দরকার, সে প্রশ্ন নয়। অণু ও পরিবেশকে একক ব্যবস্থা হিসেবে ধরলে কী ধরনের রসায়ন সম্ভব হয়, সেটিও এর অংশ।
পৃথিবীর বাইরেও এর গুরুত্ব
এ ধরনের গবেষণার স্পষ্ট অ্যাস্ট্রোবায়োলজিক্যাল মূল্য আছে। যদি জীবন আগে ধারণার তুলনায় ছোট এক জৈবরাসায়নিক উপকরণ-সেট দিয়ে শুরু হতে পারে, তবে অনুসন্ধানের যোগ্য জগতের পরিসরও বাড়তে পারে। বায়োসিগনেচার বা বসবাসযোগ্য পরিবেশ খুঁজছেন এমন বিজ্ঞানীদের সবক্ষেত্রেই আধুনিক স্থলজ জীববিজ্ঞানের প্রতিটি খুঁটিনাটি পুনরাবৃত্তি করে এমন জায়গাই খুঁজতে হবে না।
তার বদলে তারা প্রশ্ন করতে পারেন, অন্য জগতে এমন পরিস্থিতি আছে কি না যেখানে সরল পেপটাইড গঠন, একত্রিত হওয়া এবং টিকে থাকা সম্ভব। জীবনের পথে পৌঁছাতে সমসাময়িক কোষে দেখা সম্পূর্ণ সূক্ষ্মতা নাও লাগতে পারে। এটি সীমান্তবর্তী অঞ্চলেই শুরু হতে পারে, যেখানে সীমিত রসায়নও শৃঙ্খলা তৈরি করার জন্য যথেষ্ট।
এই কারণেই সরলীকৃত প্রোটিন এমন একটি কার্যকর ধারণা। এটি বিজ্ঞানের অন্যতম বৃহৎ প্রশ্নকে এমন পরীক্ষায় নামিয়ে আনে, যা এখনই করা যায়। জীববিজ্ঞানকে ছোট বর্ণমালায় নামিয়ে এনে গবেষকেরা খুঁজে পাচ্ছেন যে রসায়ন ও জীবনের মধ্যে দূরত্ব বর্তমান দৃষ্টিকোণ থেকে যতটা মনে হয়, তার চেয়ে কম হতে পারে।
- গবেষকেরা প্রায় 7 থেকে 14টি নির্মাণ উপাদানবিশিষ্ট কমানো অ্যামিনো অ্যাসিড সেট দিয়ে তৈরি প্রোটিন পরীক্ষা করছেন।
- পর্যালোচনাটি বলছে, প্রায় দশটি অ্যামিনো অ্যাসিড প্রাথমিক প্রোটিন কাঠামোকে সমর্থন করার জন্য যথেষ্ট হতে পারে।
- পরীক্ষায় দেখা গেছে, সরল পেপটাইড কার্যকরী সমমিত গঠনে একত্রিত হতে পারে।
- এই কাজের জীবন-উৎপত্তি গবেষণা এবং অ্যাস্ট্রোবায়োলজিতে উভয় ক্ষেত্রেই প্রভাব আছে।
এই নিবন্ধটি Universe Today-এর প্রতিবেদনের ভিত্তিতে রচিত। মূল নিবন্ধটি পড়ুন.