العلاجات الجينية المصممة حسب الطلب تنتقل من النظرية إلى التطبيق
لم تعد الأمراض النادرة لدى الأطفال تُعامل بوصفها مجرد غرائب علمية. ففي رسالة جديدة نُشرت في Nature Medicine، يجادل فريق من الباحثين بأنها باتت على نحو متزايد مرشحة للعلاجات الخلوية والجينية المصممة خصيصًا، بما في ذلك العلاجات المصممة لمريض واحد.
ويشير المؤلفون إلى تحول حديث لافت. فالاضطرابات الوراثية التي كانت في السابق غير قابلة للعلاج عمليًا أصبحت الآن تشهد علاجات جينية تُعطى مرة واحدة وتُحقق فوائد ذات مغزى ودائمة. وهذا التحول مهم في حد ذاته، لكن الورقة ترى أن الاضطراب الأكبر بنيوي: إذ تواجه الهيئات التنظيمية والمطورون وأنظمة الصحة الآن أدوية لا تتوافق مع افتراضات تطوير الدواء التقليدي.
وبحسب الرسالة، لم تعد التجارب الخاصة بمريض واحد فرضية نظرية. ويستشهد المؤلفون بمرض عصبي نادر للغاية جرى فيه تطوير علاج جيني قائم على فيروس مرتبط بالغدة مصمم خصيصًا للمريض ثم إعطاؤه خلال ثلاث سنوات. كما يسلطون الضوء على حالة أسرع حتى، حيث جرى إنشاء علاج تحرير القواعد الخاص بمريض بعينه، والحصول على موافقة الجهات التنظيمية عليه، وتسليمه إلى مولود جديد يعاني اضطرابًا أيضيًا مميتًا في نحو ثمانية أشهر.
وتشير هذه الأمثلة إلى أن الجانب العلمي والتصنيعي من العلاج الفردي يتقدم بسرعة. أما المشكلة الأصعب، كما يقول المؤلفون، فهي بناء مسار يمكنه جعل هذه العلاجات في متناول مزيد من الأطفال، لا مجرد عدد قليل من الحالات الاستثنائية.
مشكلة الوصول أصبحت اقتصادية بقدر ما هي علمية
تضع الرسالة مسألة الوصول بوصفها عنق الزجاجة الأساسي. فحتى مع ازدياد جدوى العلاجات الجينية المخصصة، لا يزال معظم الأطفال المصابين بأمراض نادرة لا يحصلون على علاج فعال. ولا تصف الورقة هذه الفجوة بأنها فشل علمي فقط. بل ترى أن النموذج التجاري التقليدي للأدوية غير ملائم للعلاجات شديدة الفردية.
هذا التباين ظاهر بالفعل في السوق. ويشير المؤلفون إلى أن شركات التكنولوجيا الحيوية التي ساعدت في ريادة العلاجات الجينية واجهت صعوبة في البقاء مجدية تجاريًا، وفي بعض الحالات سحبت منتجات رغم فعاليتها المنقذة للحياة. وبعبارة أخرى، لا تتمثل المشكلة فقط في ما إذا كان العلاج يمكن أن ينجح، بل في ما إذا كانت المؤسسات المصممة لتمويل العلاجات والموافقة عليها وتصنيعها واستدامتها قادرة على دعم منتجات تستهدف أعدادًا صغيرة للغاية من المرضى، أو حتى طفلًا واحدًا.
وهذا يخلق تناقضًا في قلب المجال. فكلما كان العلاج أكثر دقة وتخصيصًا، أصبح أقل شبهًا بنوع المنتج القابل للتوسع الذي صُمم نموذج الدواء التقليدي القائم على الربح ليكافئه. بالنسبة للأمراض الشائعة، يمكن للتجارب الكبيرة والأسواق الواسعة أن تبرر سنوات من الاستثمار. أما بالنسبة للاضطرابات الأطفال فائقة الندرة، فقد يتحول النموذج نفسه إلى عائق بدل أن يكون محركًا.
وتجادل الرسالة بأنه ما لم يتغير النظام، فقد تستمر العلاجات الفردية في الظهور على شكل اختراقات معزولة بدلًا من أن تصبح فئة علاجية موثوقة.
إطار يهدف إلى سد الفجوة بين التطوير والتنظيم
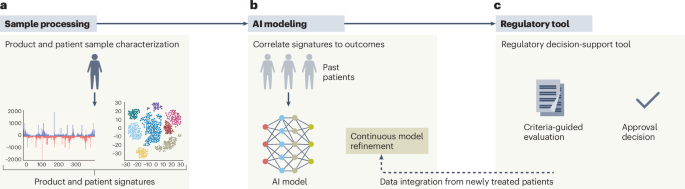
تقدم الورقة ما تسميه إطار UNICORN، بوصفه مسارًا من توصيف المنتج إلى اتخاذ القرار التنظيمي. ولا يوضح المقتطف المتاح من الرسالة هنا كل التفاصيل التشغيلية لهذا الإطار، لكن الغرض منه واضح من حجة المؤلفين: إنشاء بنية قابلة للتكرار لتقييم العلاجات الجينية المصممة خصيصًا من دون إجبارها على المرور عبر مسارات الموافقة المصممة لأدوية السوق الواسع.
وهذا مهم لأن النموذج القياسي يعتمد بدرجة كبيرة على مجموعات كبيرة، ودفعات تصنيع قابلة للتكرار، وتحقق تجاري واسع. وقد لا تتوافر أي من هذه السمات في علاجات الأطفال فائقة الندرة. ولا يزال على الجهة التنظيمية أن توازن بين الجودة والسلامة والفائدة المحتملة، لكن حزمة الأدلة قد تحتاج إلى أن تبدو مختلفة عندما يُصمم العلاج حول طفرة طفل واحد وجدوله الزمني ومساره السريري.
ولذلك تشير الرسالة إلى نموذج أكثر قابلية للتكيف، نموذج يمكنه ربط توصيف المنتج بالمراجعة التنظيمية بطريقة تحافظ على الصرامة مع الإقرار بأن العلاجات الفردية منتجات مختلفة جوهريًا.
والرسالة الضمنية ليست أن المعايير ينبغي أن تُضعف، بل إنها قد تحتاج إلى أن تُترجم إلى صيغة جديدة. فإذا صُنعت علاجات لمريض واحد، فلا يمكن لمنطق الموافقة أن يعتمد على الافتراضات نفسها المستخدمة لمنتج موجه لعشرات الآلاف.
لماذا تُعد أمراض الأطفال النادرة نقطة الضغط
تُعد أمراض الأطفال النادرة المكان الذي يبلغ فيه هذا الضغط ذروته. فالمرضى قليلون، وقد يكون التقدم سريعًا، ويمكن للتأخير أن يترك عواقب مدى الحياة. وتبرز الأمثلة التي استشهد بها المؤلفون هذه العجلة. فجدول تطوير يمتد ثلاث سنوات لعلاج مصمم خصيصًا يُعد بالفعل مكثفًا للغاية بمقاييس تطوير الدواء التاريخية. أما المسار الذي انتقل من التصميم إلى الموافقة التنظيمية ثم إلى علاج مولود جديد في نحو ثمانية أشهر فهو أكثر درامية.
وتُظهر هذه الجداول الزمنية كلًا من وعد هذا المجال وهشاشته. فهي تثبت أن العلاجات المصممة حسب الطلب يمكن أن تتحرك بسرعة ملحوظة عندما تتوافق العلوم والتصنيع والتنظيم والحاجة السريرية. كما أنها تطرح سؤالًا صعبًا: إذا كان هذا ممكنًا في الحالات الاستثنائية، فما الذي يتطلبه تحويله إلى ممارسة منهجية؟
وتجادل الرسالة بأن الإجابة ليست مجرد مزيد من الابتكار المخبري، بل أيضًا تصميم مؤسسي أفضل. فكثيرًا ما لا توجد للأمراض النادرة لدى الأطفال علاجات بديلة ولا سوق تجاري كبير. وهذا يجعلها حالة اختبار لمعرفة ما إذا كان الطب قادرًا على بناء أنظمة تطوير تتمحور حول الحاجة لا الحجم.
ما الذي تشير إليه هذه المقترحات بالنسبة للمجال
تكمن أهمية الورقة أقل في الإعلان عن علاج واحد وأكثر في الإقرار بأن فئة دوائية جديدة تصل أسرع مما تستطيع الأنظمة القديمة استيعابه. ويصف المؤلفون عالمًا تصبح فيه العلاجات الجينية المصممة حسب الطلب ممكنة تقنيًا وذات معنى سريريًا، ومع ذلك يصعب تسليمها بنيويًا.
إذا ثبتت حجتهم، فإن التقدم المستقبلي في أمراض الأطفال النادرة لن يعتمد فقط على نواقل أفضل أو أدوات تحرير أو طرق تصنيع أفضل، بل أيضًا على مسارات موافقة تعترف بالعلاجات الفردية بوصفها واقعًا دائمًا. وتقول الرسالة إن طب الأمراض النادرة دخل بالفعل هذه المرحلة.
وهذا تحول مهم. فلعقود، كانت العلاجات الجينية الشخصية تبدو غالبًا كطموح في حدود الممكن. أما الأمثلة المذكورة هنا فتشير إلى أنها أصبحت الآن تحديًا إداريًا وتنظيميًا بقدر ما هي تحدٍ علمي. وقد تعتمد الاختراقات التالية على قدرة الجهات التنظيمية والمطورين على تحويل النجاحات الفردية إلى نظام قابل للعمل.
وبالنسبة للعائلات التي تواجه اضطرابات طفولية مدمرة، فهذا التمييز ليس مجرد مسألة نظرية. فقد يحدد ما إذا كان الطب المصمم خصيصًا سيبقى الاستثناء، أم سيبدأ في أن يصبح جزءًا من الرعاية الروتينية للأمراض النادرة للغاية بحيث لا تناسب النموذج القديم.
هذه المقالة تستند إلى تقرير من Nature Medicine. اقرأ المقال الأصلي.
Originally published on nature.com