जीन-संपादित ट्रांसप्लांट दृष्टिकोण ने शुरुआती क्लिनिकल पड़ाव छुआ
Nature Medicine में प्रकाशित पहली-मानव अध्ययन उच्च-जोखिम acute myeloid leukemia और myelodysplastic syndrome वाले रोगियों के लिए तैयार CRISPR-Cas9-संपादित allogeneic hematopoietic cell transplant के शुरुआती क्लिनिकल परिणाम प्रस्तुत करता है। यह उपचार रणनीति ऐसे donor cells का उपयोग करती है जिनमें CD33 target हटाया गया है; इससे डॉक्टर सामान्य donor-derived myeloid cells को समान स्तर के जोखिम में डाले बिना transplant के बाद CD33-directed दवा gemtuzumab ozogamicin दे सकते हैं।
इस दृष्टिकोण के पीछे का तर्क सीधा है, लेकिन तकनीकी रूप से बेहद महत्वाकांक्षी। उच्च-जोखिम AML या MDS वाले रोगियों में allogeneic hematopoietic cell transplantation के बाद भी relapse हो सकता है। post-transplant maintenance में एक चुनौती यह है कि residual leukemia को दबाने या खत्म करने के लिए दी जाने वाली therapies स्वस्थ donor cells को भी नुकसान पहुँचा सकती हैं। इस trial का investigational product tremtelectogene empogeditemcel, या trem-cel, infusion से पहले donor graft से CD33 हटाकर इस समस्या का एक हिस्सा हल करने का लक्ष्य रखता है।
phase 1/2a trial में क्या मिला
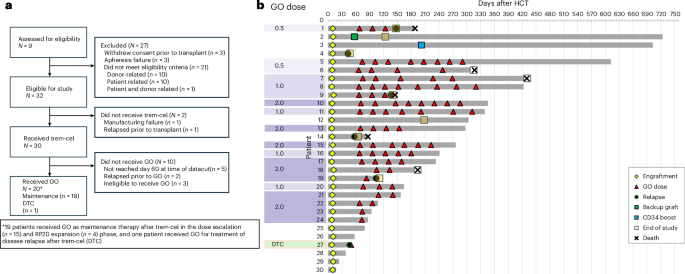
बहु-केंद्र, open-label phase 1/2a अध्ययन में relapse के उच्च जोखिम वाले AML या MDS वाले वयस्क रोगियों को शामिल किया गया। myeloablative conditioning के बाद रोगियों को trem-cel दिया गया। इसके बाद कुछ प्रतिभागियों को 28-दिवसीय चक्रों में 0.5 mg/m2 से 2.0 mg/m2 की खुराकों पर maintenance gemtuzumab ozogamicin दिया गया।
मुख्य safety endpoint day 28 तक neutrophil engraftment था। प्रकाशित रिपोर्ट के अनुसार, trem-cel पाने वाले सभी 30 रोगियों ने यह endpoint हासिल किया। neutrophil engraftment का median समय 10 दिन था, 95% confidence interval 9 से 10 दिन। यह महत्वपूर्ण है, क्योंकि delayed या failed engraftment किसी भी transplant रणनीति में, और खासकर genome-edited donor cells वाली प्रणाली में, मुख्य जोखिमों में से एक है।
19 रोगियों को post-transplant gemtuzumab ozogamicin maintenance मिला, जिनमें 15 phase 1 dose-escalation भाग में और 4 phase 2 dose expansion में थे। अध्ययन बताता है कि gemtuzumab ozogamicin recommended phase 2 dose 2 mg/m2 तक सुरक्षित रूप से सहन हुआ। paper यह भी नोट करता है कि trial जल्दी बंद कर दिया गया था और यह पूर्ण phase 1 भाग सहित अंतिम रिपोर्ट है।