Un alphabet plus petit pour une question plus vaste
L’un des problèmes les plus difficiles de la science est aussi l’un des plus anciens : comment la chimie inerte de la Terre primitive a donné naissance à la biologie. Un nouvel article de synthèse mis en avant par Universe Today aborde cette question par une voie étonnamment concrète. Plutôt que d’essayer de reconstituer toute la complexité des protéines modernes, les chercheurs testent si des versions beaucoup plus simples pouvaient se replier, fonctionner et résister dans des conditions prébiotiques.
L’article, intitulé The borderlands of foldability: lessons from simplified proteins et publié dans Trends in Chemistry, se concentre sur ce que l’on appelle les protéines simplifiées. Le principe central est simple. Les protéines modernes sont constituées de 20 acides aminés distincts, mais la Terre primitive ne disposait probablement pas de toute cette boîte à outils. Si les premiers peptides et protéines n’avaient accès qu’à un sous-ensemble plus réduit, alors l’émergence de la vie a peut-être dépendu de beaucoup moins d’informations biochimiques que n’en exigent les organismes modernes.
Pourquoi la biologie moderne peut être trompeuse
Les protéines des systèmes vivants actuels sont des molécules hautement complexes dont la forme est au cœur de leur fonction. Elles se replient en structures tridimensionnelles qui permettent aussi bien la catalyse que le soutien structurel. Regarder en arrière à partir d’une telle complexité peut donner une image trompeuse de la difficulté des premières étapes.
La revue soutient que les premiers peptides étaient probablement courts et simples, composés d’acides aminés présents naturellement dans l’environnement ou produits par un métabolisme extrêmement primitif. Les chercheurs ne peuvent pas récupérer des fossiles de protéines anciennes pour le confirmer directement, mais l’article considère cela comme un point de départ raisonnable pour le travail expérimental.
C’est là qu’intervient la « réduction de l’alphabet ». Les scientifiques reconstruisent des protéines à l’aide d’alphabets restreints d’environ sept à 14 acides aminés plutôt que les 20 standard. L’objectif n’est pas de créer des approximations grossières de la biologie moderne. Il s’agit de tester si un vocabulaire chimique plus simple peut encore produire des structures ordonnées et fonctionnelles.
Se replier avec moins d’ingrédients
Les résultats décrits dans la revue sont frappants. Les scientifiques sont parvenus à construire des protéines qui se replient en structures tridimensionnelles stables tout en excluant des classes entières de blocs de construction plus complexes. Autrement dit, une grande partie de la logique architecturale nécessaire à la formation des protéines semble ne pas dépendre de l’ensemble moderne complet des acides aminés.
Cette découverte est importante parce qu’elle abaisse la barrière apparente à l’émergence de la vie. Si un alphabet « prébiotique » d’environ dix acides aminés suffit à faire émerger des protéines structurées, alors la Terre primitive n’aurait pas eu besoin de résoudre d’un seul coup le problème moderne des protéines. Elle avait seulement besoin d’assez de chimie pour produire des molécules capables de s’organiser elles-mêmes en formes utiles.
La revue présente cela comme la preuve que les architectures fondamentales nécessaires à la biologie peuvent émerger à partir d’une information étonnamment limitée. Cela n’explique pas la transition complète de la chimie à la vie, mais cela resserre l’une des dimensions les plus intimidantes de cet écart.
Une vieille hypothèse gagne un soutien expérimental
Le texte source renvoie à une proposition bien connue de 1966 formulée par Richard Eck et Margaret Dayhoff, qui suggéraient que d’anciennes protéines symétriques auraient pu se former par duplication et fusion de peptides courts et simples. Les travaux modernes semblent désormais soutenir cette idée en pratique.
Des chercheurs ont observé que de simples peptides « homo-oligomérisent », s’assemblant effectivement pour former des protéines symétriques et fonctionnelles. L’image est importante parce que la symétrie offre un raccourci plausible. Les systèmes primitifs n’avaient peut-être pas besoin, dès le départ, de séquences longues et précisément codées. La répétition de petits modules aurait pu suffire à créer des structures ayant une véritable capacité.
Cette vision donne à la recherche sur l’origine de la vie un modèle plus progressif. Au lieu d’imaginer un saut soudain de la chimie aléatoire à des protéines hautement raffinées, les scientifiques peuvent explorer comment de modestes assemblages de peptides courts ont pu accumuler des fonctions au fil du temps.
L’environnement a peut-être fait partie du mécanisme
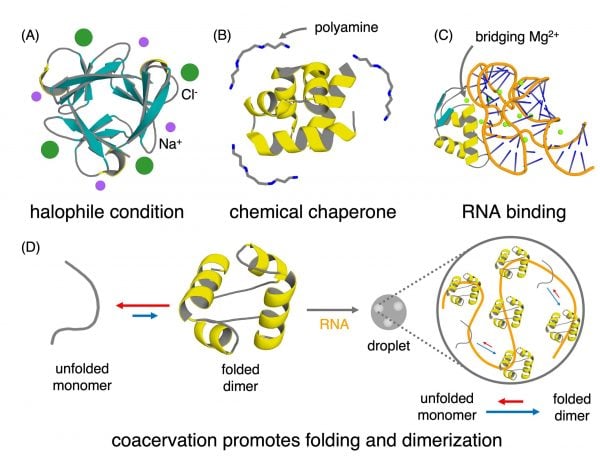
La revue souligne également que les premières protéines ne seraient pas apparues isolément. L’environnement alentour a peut-être activement aidé à leur survie et à leur repliement. C’est un changement de perspective crucial. Dans la biologie moderne, les cellules contrôlent étroitement les conditions internes. Sur la Terre primitive, en revanche, les minéraux, les sels, les surfaces et les contextes chimiques locaux ont peut-être joué un rôle d’échafaudage ou de stabilisateurs.
Si cela est exact, les premières protéines utiles ont peut-être été plus simples non seulement parce que leur alphabet d’acides aminés était plus petit, mais aussi parce que l’environnement faisait une partie du travail. Un peptide qui semble marginal dans un contexte de laboratoire moderne aurait pu se comporter très différemment dans une niche prébiotique favorable.
Cette dimension environnementale élargit l’importance des études sur les protéines simplifiées. Elles ne portent pas seulement sur les informations de séquence nécessaires. Elles portent aussi sur ce que la chimie permet lorsque les molécules et le milieu sont considérés comme un seul système.
Pourquoi cela compte au-delà de la Terre
Ce type de recherche a une valeur astrobiologique évidente. Si la vie peut commencer avec une boîte à outils biochimique plus réduite qu’on ne le pensait, alors l’éventail des mondes à étudier peut s’élargir. Les scientifiques qui recherchent des biosignatures ou des environnements habitables n’ont pas nécessairement besoin de chercher des lieux reproduisant chaque détail de la biologie terrestre moderne.
Ils peuvent plutôt se demander si d’autres mondes offrent des conditions où de simples peptides peuvent se former, s’assembler et persister. Le chemin vers la vie n’exige peut-être pas toute la sophistication observée dans les cellules contemporaines. Il peut commencer dans les zones frontières, où une chimie limitée suffit encore à générer de l’ordre.
C’est pourquoi les protéines simplifiées constituent une idée si utile. Elles réduisent l’une des plus grandes questions de la science à des expériences réalisables dès maintenant. En ramenant la biologie à un alphabet plus petit, les chercheurs découvrent que la distance entre la chimie et la vie a peut-être été plus courte qu’elle n’en a l’air depuis le point de vue actuel.
- Les chercheurs testent des protéines construites avec des alphabets d’acides aminés réduits d’environ sept à 14 briques.
- La revue soutient qu’une dizaine d’acides aminés pourrait avoir suffi à soutenir les architectures protéiques précoces.
- Les expériences montrent que de simples peptides peuvent s’auto-assembler en structures symétriques et fonctionnelles.
- Ces travaux ont des implications pour la recherche sur l’origine de la vie et pour l’astrobiologie.
Cet article est basé sur un reportage de Universe Today. Lire l’article original.