Une nouvelle frontière dans le traitement du cancer
Les vaccins contre le cancer occupent une position unique dans l'histoire de la médecine : un concept thérapeutique qui a été poursuivi pendant plus d'un siècle mais qui n'a acquis que récemment la compréhension biologique et les outils technologiques nécessaires pour le rendre efficace de manière cliniquement significative. Un examen complet publié dans Nature Medicine examine où en est le domaine aujourd'hui, retraçant le chemin des premiers revers aux approches sophistiquées basées sur mRNA et ciblant les néoantigènes qui progressent maintenant dans les essais cliniques avec une véritable promesse.
Le calendrier de l'examen reflète une véritable accélération dans le domaine. Les plates-formes technologiques mRNA qui ont alimenté les vaccins COVID-19 ont été adaptées aux applications contre le cancer avec une vitesse remarquable, et les données cliniques précoces des programmes de vaccins contre le cancer personnalisés ont été suffisamment encourageantes pour attirer des milliards de dollars d'investissement de sociétés pharmaceutiques qui ont été longtemps skeptiques face à la viabilité commerciale de la vaccination contre le cancer. Le paysage en 2026 est fondamentalement différent de celui d'il y a à peine cinq ans.
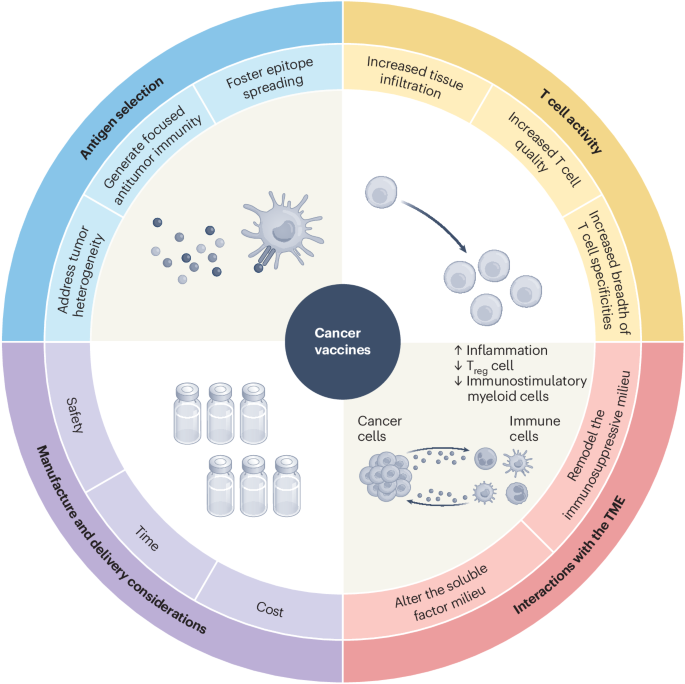
Les vaccins contre le cancer fonctionnent selon un principe différent de celui des vaccins traditionnels contre les maladies infectieuses. Plutôt que d'entraîner le système immunitaire à reconnaître un pathogène avant l'exposition, les vaccins contre le cancer visent à entraîner le système immunitaire à reconnaître et détruire les cellules tumorales qui sont déjà présentes dans le corps. Cette approche de vaccination thérapeutique nécessite d'identifier précisément les cibles moléculaires sur les cellules tumorales qui les marquent comme étrangères et de générer une réponse immunitaire suffisamment puissante pour surmonter l'environnement immunosuppresseur que les tumeurs créent pour se protéger de l'élimination immunitaire.
Vaccins contre le cancer personnalisés basés sur mRNA
L'approche de vaccin contre le cancer la plus avancée scientifiquement actuellement en développement clinique utilise la technologie mRNA pour créer des vaccins personnalisés ciblant les néoantigènes - des fragments de protéines mutantes qui sont uniques à la tumeur d'un patient individuel. Parce que ces cibles sont créées par les mutations spécifiques dans les cellules cancereuses de chaque patient, elles ne sont pas présentes sur le tissu normal, ce qui en fait des cibles hautement sélectives pour l'attaque immunitaire.
Le processus de développement des vaccins personnalisés implique le séquençage de la tumeur d'un patient pour identifier ses mutations spécifiques, l'utilisation d'outils computationnels pour prédire quels peptides mutants seront affichés sur les surfaces des cellules tumorales et reconnus par les cellules immunitaires, la synthèse d'un vaccin mRNA codant ces cibles et l'administration du vaccin pour stimuler une réponse immunitaire. L'ensemble du processus, du séquençage tumoral à l'administration du vaccin, prend maintenant des semaines dans les environnements de fabrication avancés, contre des mois il y a à peine quelques années.
Moderna et Merck ont mené le développement clinique dans cet espace avec leur candidat mRNA-4157, qui en combinaison avec l'inhibiteur de point de contrôle pembrolizumab a montré une réduction statistiquement significative des récidives de mélanome dans un essai randomisé de Phase 2 - un résultat qui a électrisé le domaine et a été suivi par une expansion à plusieurs types de cancer. L'examen de Nature Medicine place ce résultat dans le contexte d'un domaine plus large qui évalue maintenant les vaccins mRNA personnalisés sur le cancer du poumon, colorectal, de la vessie et d'autres types de cancer.
Vaccins contre l'antigène partagé et approches combinées
Tous les programmes de vaccins contre le cancer ne sont pas personnalisés. Les vaccins contre l'antigène partagé ciblent des protéines surexprimées dans les tumeurs de nombreux patients - des cibles comme HER2, MAGE et les antigènes glucidiques associés aux tumeurs qui sont suffisamment courants pour soutenir le développement de produits prêts à l'emploi avec une fabrication potentiellement plus simple et à coût inférieur. Ces approches échangent une partie de la spécificité des néoantigènes personnalisés contre les avantages pratiques d'une production évolutive et d'un développement clinique standardisé.
Les approches combinées associant les vaccins contre le cancer aux inhibiteurs de point de contrôle, aux thérapies CAR-T ou à d'autres modalités d'immunothérapie sont devenues un domaine majeur d'investigation. Le fondement logique est que les vaccins stimulent les réponses immunitaires ciblant les tumeurs tandis que les inhibiteurs de point de contrôle éliminent les freins que les tumeurs utilisent pour supprimer ces réponses - produisant potentiellement une activité antitumorale synergique qu'aucune approche ne peut réaliser seule. Les données cliniques de ces combinaisons s'accumulent sur plusieurs types de tumeurs.
L'examen souligne la sophistication croissante des systèmes d'administration des vaccins, notamment les nanoparticules lipidiques optimisées pour la présentation des antigènes tumoraux, les nouvelles formulations d'adjuvants qui améliorent l'activation immunitaire sans toxicité excessive, et les approches programmables in vivo qui génèrent des réponses immunitaires personnalisées en utilisant la machinerie cellulaire endogène plutôt que les étapes de fabrication ex vivo.
Défis et questions ouvertes
Malgré des progrès véritables, le domaine des vaccins contre le cancer fait face à des défis importants que l'examen de Nature Medicine aborde directement. L'évasion immunitaire tumorale - la capacité des cellules cancereuses à réduire l'expression d'antigènes, créer des microenvironnements immunosuppresseurs et développer une résistance à l'attaque immunitaire - reste un obstacle fondamental. Les vaccins qui génèrent de fortes réponses immunitaires initiales pourraient encore ne pas produire un contrôle tumoral durable si la tumeur évolue pour échapper à la réponse immunitaire qu'ils stimulent.
La sélection des patients reste imparfaitement comprise. Certains types de tumeurs et certains patients semblent réagir de manière spectaculaire aux approches de vaccin contre le cancer, tandis que d'autres montrent un bénéfice minimal, et les prédicteurs biologiques de la réponse ne sont pas encore suffisamment caractérisés pour guider les décisions de traitement avec confiance. L'identification des biomarqueurs qui prédisent la réponse au vaccin est une priorité de recherche majeure dans l'ensemble du domaine.
Les coûts de fabrication et la complexité, particulièrement pour les vaccins personnalisés, restent un obstacle à l'accès large. Le processus de séquençage d'une tumeur, d'identification des cibles, de conception et de synthèse d'un vaccin individualisé et de son administration dans un délai cliniquement pertinent implique une infrastructure substantielle et reste coûteux. Réduire ces coûts par l'innovation des procédés et l'augmentation de la fabrication sera nécessaire pour que les vaccins contre le cancer personnalisés atteignent leur plein potentiel de population de patients.
La voie à suivre
L'examen de Nature Medicine conclut avec un optimisme mesuré sur la trajectoire du domaine. Plusieurs essais de Phase 3 sont maintenant en cours pour des candidats vaccins contre le cancer dans des contextes où les données de Phase 2 ont été suffisamment convaincantes pour justifier l'investissement. Les résultats de ces essais plus importants arriveront au cours des prochaines années et détermineront largement la rapidité avec laquelle les vaccins contre le cancer passent du traitement expérimental au traitement standard dans la pratique oncologique.
La convergence de la technologie de plate-forme mRNA, de la prédiction des néoantigènes assistée par IA, du séquençage rapide des tumeurs et de la compréhension de plus en plus sophistiquée de l'immunologie tumorale a créé les conditions permettant aux vaccins contre le cancer de réussir de manières que les générations précédentes de chercheurs ne pouvaient pas réaliser. Que le domaine livre finalement la promesse de transformer le système immunitaire en un traitement du cancer largement applicable reste à voir, mais les preuves cliniques sont maintenant suffisamment solides pour prendre cette possibilité au sérieux.
Cet article est basé sur les rapports de Nature Medicine. Lire l'article original.