حدود جديدة في علاج السرطان
تحتل لقاحات السرطان مكاناً فريداً في تاريخ الطب: مفهوم علاجي تم السعي وراءه لأكثر من قرن، لكنه حصل فقط مؤخراً على الفهم البيولوجي والأدوات التكنولوجية اللازمة لجعله يعمل بطريقة ذات معنى سريري. يفحص استعراض شامل نُشر في Nature Medicine الحالة الحالية للمجال، يتتبع الطريق من الانتكاسات المبكرة إلى طرق mRNA المتطورة والموجهة للمستضدات الجديدة التي تتقدم الآن عبر التجارب السريرية بوعود حقيقية.
يعكس توقيت الاستعراض تسارعاً حقيقياً في المجال. تم تكييف منصات تقنية mRNA التي دعمت لقاحات COVID-19 لتطبيقات السرطان بسرعة ملحوظة، والبيانات السريرية المبكرة من برامج لقاحات السرطان الشخصية كانت مشجعة بما يكفي لجذب مليارات الدولارات في الاستثمارات من شركات الأدوية التي ظلت متشككة لسنوات في الجدوى التجارية للقاحات السرطان. المشهد في عام 2026 مختلف بشكل أساسي عما كان عليه قبل خمس سنوات فقط.
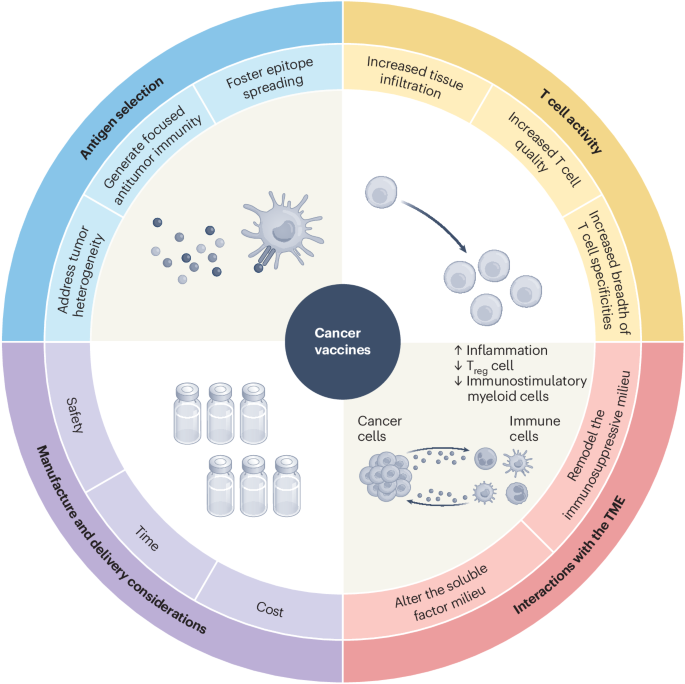
تعمل لقاحات السرطان على مبدأ مختلف عن اللقاحات التقليدية للأمراض المعدية. بدلاً من تدريب الجهاز المناعي على التعرف على مسبب الأمراض قبل التعرض، تهدف لقاحات السرطان إلى تدريب الجهاز المناعي على التعرف على خلايا الورم والقضاء عليها التي موجودة بالفعل في الجسم. يتطلب هذا النهج اللقاحي العلاجي تحديد دقيق للأهداف الجزيئية على خلايا الورم التي تميزها كغريبة وإنتاج استجابة مناعية قوية بما يكفي للتغلب على البيئة المثبطة للمناعة التي ينشئها الورم لحماية نفسه من القضاء المناعي.
لقاحات السرطان الشخصية القائمة على mRNA
يستخدم أكثر نهج متقدم علمياً لقاح السرطان قيد التطوير السريري الآن تقنية mRNA لإنشاء لقاحات شخصية تستهدف المستضدات الجديدة - جزيئات البروتين الطفرية التي تكون فريدة لورم كل مريض على حدة. لأن هذه الأهداف يتم إنشاؤها بواسطة الطفرات المحددة في خلايا السرطان لدى كل مريض، فهي غير موجودة في الأنسجة الطبيعية، مما يجعلها أهدافاً انتقائية جداً للهجوم المناعي.
تتضمن عملية تطوير اللقاح الشخصي تسلسل ورم المريض لتحديد طفراته المحددة، واستخدام أدوات حسابية للتنبؤ بأي الببتيدات الطفرية سيتم عرضها على سطح خلايا الورم والتعرف عليها من قبل الخلايا المناعية، وتصنيع لقاح mRNA يشفر تلك الأهداف، وإعطاء اللقاح لتحفيز استجابة مناعية. تستغرق خط أنابيب الكامل بأكمله، من تسلسل الورم إلى إعطاء اللقاح، أسابيع الآن في بيئات التصنيع المتقدمة، نزولاً من أشهر قبل بضع سنوات فقط.
قادت Moderna و Merck التطوير السريري في هذا المجال مع مرشحهما mRNA-4157، الذي أظهر في تركيبة مع مثبط نقطة التفتيش pembrolizumab تقليلاً ذا دلالة إحصائية في انتكاس الورم الميلانيني في تجربة عشوائية في المرحلة الثانية - نتيجة أثارت فرح المجال وتم متابعتها بالتوسع إلى أنواع سرطان متعددة. يضع استعراض Nature Medicine هذه النتيجة في سياق مجال أوسع يقيّم الآن لقاحات mRNA الشخصية عبر سرطان الرئة والقولون والمثانة وأنواع سرطان أخرى.
لقاحات المستضد المشترك والنهج المركبة
لا تكون جميع برامج لقاح السرطان شخصية. تستهدف لقاحات المستضد المشترك البروتين الذي يتم الإفراط في التعبير عنه عبر أورام العديد من المرضى - أهداف مثل HER2 و MAGE والمستضدات الكربوهيدراتية المرتبطة بالورم التي شائعة بما يكفي لدعم تطوير المنتجات الجاهزة مع التصنيع المحتمل الأبسط والتكلفة الأقل. تتنازل هذه الأنهج عن بعض خصوصية المستضدات الجديدة الشخصية مقابل المزايا العملية للإنتاج القابل للتوسع والتطوير السريري الموحد.
ظهرت النهج المركبة التي تجمع بين لقاحات السرطان ومثبطات نقطة التفتيش أو علاجات CAR-T أو طرق العلاج المناعي الأخرى كمجال تحقيق رئيسي. الأساس المنطقي هو أن اللقاحات تهيئ استجابات مناعية موجهة نحو الورم بينما تزيل مثبطات نقطة التفتيش الفرامل التي يستخدمها الورم لقمع تلك الاستجابات - ربما تنتج نشاطاً مضاداً للورم متناغماً لا يحققه أي من النهجين وحده. البيانات السريرية من هذه المركبات تتراكم عبر أنواع أورام متعددة.
يسلط الاستعراض الضوء على التطور المتزايد لأنظمة توصيل اللقاح، بما في ذلك الجزيئات النانوية الدهنية المحسنة لعرض مستضد الورم، وصيغ المساعد الصحي الجديدة التي تعزز التنشيط المناعي دون سمية مفرطة، والنهج القابلة للبرمجة في الجسم الحي التي تولد استجابات مناعية شخصية باستخدام الآلية الخلوية الموجودة بدلاً من خطوات التصنيع خارج الجسم الحي.
التحديات والأسئلة المفتوحة
على الرغم من التقدم الحقيقي، يواجه مجال لقاح السرطان تحديات كبيرة يعالجها استعراض Nature Medicine بشكل مباشر. يعتبر الإفلات المناعي للورم - القدرة على تقليل التعبير عن المستضد وخلق بيئات مثبطة للمناعة والتطور ليصبح مقاوماً للهجوم المناعي - حاجزاً أساسياً متبقياً. قد لا تزال اللقاحات التي تولد استجابات مناعية قوية في البداية تفشل في إنتاج السيطرة على الورم الدائمة إذا تطور الورم ليتجنب الاستجابة المناعية التي يحفزها.
لا تزال عملية اختيار المريض غير مفهومة بشكل كامل. يبدو أن بعض أنواع الأورام وبعض المرضى يستجيبون بشكل درامي لنهج لقاح السرطان، بينما يظهر آخرون فائدة ضئيلة جداً، والمؤشرات البيولوجية للاستجابة لم تكن معروفة بعد بشكل كافٍ لتوجيه قرارات العلاج بثقة. يعتبر تحديد المؤشرات الحيوية التي تتنبأ باستجابة اللقاح أولوية بحثية رئيسية عبر المجال.
تبقى تكاليف التصنيع والتعقيد، خاصة بالنسبة للقاحات الشخصية، عقبة أمام الوصول الواسع. تتضمن عملية تسلسل ورم المريض وتحديد الأهداف وتصميم وتصنيع لقاح فردي وإعطاؤه ضمن إطار زمني ذي معنى سريري بنية تحتية كبيرة وتبقى مكلفة. سيكون من الضروري خفض هذه التكاليف من خلال الابتكار في العملية والتوسع في التصنيع لكي تصل لقاحات السرطان الشخصية إلى إمكانياتها الكاملة لسكان المرضى.
الطريق إلى الأمام
يختتم استعراض Nature Medicine بتفاؤل معتدل حول مسار المجال. عدة تجارب في المرحلة الثالثة جارية الآن لمرشحي لقاح السرطان في إعدادات حيث البيانات من المرحلة الثانية كانت مقنعة بما يكفي لتبرير الاستثمار. ستصل نتائج هذه التجارب الأكبر على مدى السنوات القادمة وستحدد بشكل كبير مدى السرعة التي تنتقل بها لقاحات السرطان من علاج تجريبي إلى علاج معياري في ممارسة الأورام.
كان التقارب بين تقنية منصة mRNA والتنبؤ بالمستضد الجديد المدعوم بالذكاء الاصطناعي والتسلسل السريع للورم والفهم المتطور بشكل متزايد لمناعة الورم قد أنشأ الشروط التمكينية لنجاح التطعيم ضد السرطان بطرق لم تستطع الأجيال السابقة من الباحثين تحقيقها. ما إذا كان المجال في النهاية سيحقق على وعد تحويل الجهاز المناعي إلى علاج سرطان قابل للتطبيق على نطاق واسع يبقى لينظر فيه، لكن الأدلة السريرية الآن قوية بما يكفي لأخذ تلك الإمكانية على محمل الجد.
تم نشر هذا المقال بناءً على التقارير من Nature Medicine. اقرأ المقالة الأصلية.